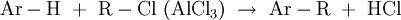Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Friedel-Crafts-AlkylierungDie Friedel-Crafts-Alkylierung (benannt nach ihren Endeckern Charles Friedel und James Mason Crafts) ist eine Reaktion in der Organischen Chemie, bei der an einem aromatischen Kohlenwasserstoff ein Wasserstoffatom gegen eine Alkylgruppe substituiert wird (→ Alkylierung). Dabei entstehen Alkylaromaten.
Produkt-Highlight
KlassifizierungDie Friedel-Crafts-Alkylierung ist eine aromatische elektrophile Substitution (SE), die nach einem Additions-Eliminierungs-Mechanismus verläuft. Dabei addiert sich ein Elektrophil (Kation oder Dipol) zunächst an den Aromaten, der dann unter Freisetzung eines Protons rearomatisiert. Edukte und KatalysatorenAls Alkylierungsreagenzien werden bei der Friedel-Crafts-Alkylierung Alkylhalogenide, Alkohole oder Alkene genutzt. Diese müssen jedoch zunächst durch Katalysatoren aktiviert werden. Als Katalysatoren werden Lewis-Säuren verwendet, die aufgrund ihrer Elektronenaffinität das Alkylierungsreagenz "positivieren", das heißt einen Dipol erzeugen oder verstärken beziehungsweise ein Kation generieren.
Neben Aluminiumchlorid werden unter anderem Phosphorsäure, Schwefelsäure, Fluorwasserstoff und Quecksilber-II-sulfat als Katalysatoren verwendet. ReaktionsablaufDas Elektrophil greift zunächst am π-Elektronensystem des Aromaten an und addiert sich dann unter Bildung einer σ-Bindung an diesen. Dabei wird vorübergehend die Aromatizität des Rings aufgehoben, der dann durch Abspaltung eines Protons rearomatisiert. MehrfachsubstitutionDa eine bereits am Aromaten vorhandene Alkylgruppe den Ring gegenüber weiteren Substitutionsreaktionen aufgrund ihres positiven induktiven Effektes (+I) aktiviert, isoliert man bei Alkylierungen nach Friedel-Crafts oft mehrfachsubstituierte Produkte. Um einfachsubstituierte Produkte zu erhalten, muss mit einem Überschuss des Aromaten gearbeitet werden, weshalb die Friedel-Crafts-Alkylierung für teure Benzolderivate nicht geeignet ist. Polyalkylaromaten können durch einen Überschuss an Alkylierungsreagenz gewonnen werden. Im Fall von Benzol ist dabei zu beachten, dass durch das Einführen eines Alkylrestes in einen unsubstituierten Ring die Äquivalenz der Positionen am Ring abhanden kommt. Substituenten haben einen sogenannten dirigierenden Einfluss auf die Position der nachfolgenden Substitutionsreaktion. Man spricht von ortho-para- beziehungsweise meta-dirigierenden Substituenten (siehe dazu: Konstitution, Konstitutionsisomerie). Die Mehrfachsubstitution ist meist unerwünscht, da aufgrund des geringen induktiven Effekts der Alkylgruppe oftmals ein Produktgemisch aus mehreren Isomeren erhalten wird. Wegen der durch jede neu hinzugefügte Alkylgruppe gesteigerten Affinität des Aromaten gegenüber Elektrophilen, ist es beispielsweise möglich, bei Hexamethylbenzol eine siebte Methylgruppe einzuführen. Die Reaktion endet dann mit einem relativ stabilen Phenoniumion.
Problem durch UmlagerungProbleme tauchen besonders bei der Umsetzung primärer Alkylhalogenide und Alkoholen auf. Das hieraus durch Einwirkung des Katalysators entstandene primäre Carbokation neigt dazu sich durch Umlagerung zu stabilisieren. Meist tritt hierbei die Wagner-Meerwein-Umlagerung auf. Das hieraus entstandene isomere Carbokation, kann nun ebenfalls als Elektrophil dienen, was zur Bildung unerwünschter Nebenprodukte führt. TransalkylierungDie Friedel-Crafts-Alkylierung ist eine reversible Reaktion. Daher lassen sich Alkylreste von Alkylaromaten durch Erhitzen und unter Einfluss eines Katalysators auf andere Aromaten übertragen. Kinetische und thermodynamische KontrolleUnter relativ milden Reaktionsbedingungen sind Alkylgruppen ortho- und para-dirigierend. Es entsteht das kinetisch-kontrollierte Endprodukt. Bei höherer Temperatur oder mit starken Lewis-Säuren entstehen bevorzugt die thermodynamisch stabileren meta-Produkte. Weiterführende InformationenFriedel-Crafts-Acylierung, Namensreaktionen, Reaktionsmechanismus |
|
| Dieser Artikel basiert auf dem Artikel Friedel-Crafts-Alkylierung aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |