Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Bariumhydroxid
Bariumhydroxid bildet weiße, salzartige Kristalle. Handelsübliches Bariumhydroxid kommt als Octahydrat Ba(OH)2 · 8 (H2O) in den Handel. Produkt-Highlight
Eigenschaften und VerhaltenBariumhydroxid ist eine feste, aus weißen Kristallen bstehende Substanz. Die Löslichkeit in Wasser ist stark temperaturabhängig, bei 20 °C lösen sich 5,6 g/l Wasser, bei 80 °C 94,7 g/l Wasser. Die wässrige Lösung, auch Barytwasser genannt, ist stark alkalisch (pH-Wert >> 7), da Bariumhydroxid fast vollständig dissoziert. Eine gesättigte Lösung hat einen pH von 14. ReaktionsverhaltenBariumhydroxid bildet in wässriger Lösung mit Kohlendioxid einen unlöslichen Niederschlag aus Bariumcarbonat: Vorkommen und GewinnungBariumhydroxid kommt nicht in der Natur vor. HerstellungAusgehend vom Schwerspat (Bariumsulfat) BaSO4 wird Bariumhydroxid aus Bariumoxid oder Bariumsulfid gewonnen: Bariumoxid reagiert mit Wasser zum Bariumhydroxid:
Verwendung
Quellen
Kategorien: Ätzender Stoff | Hydroxid | Base | Bariumverbindung |
|||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Bariumhydroxid aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | |||||||||||||||||||||||||||||||||||||||||||||






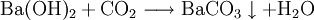
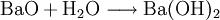 ,
,
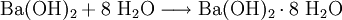 .
.
 .
.


