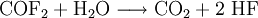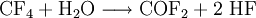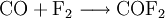Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Carbonylfluorid
Carbonylfluorid ist die gebräuchlichste Bezeichnung für Kohlenoxiddifluorid, COF2, dem Difluorid der Kohlensäure. Es ist das Fluor-Analogon des Phosgens. Produkt-Highlight
EigenschaftenCarbonylfluorid ist ein giftiges, stechend riechendes Gas, das aufgrund seiner Hygroskopie an der Luft raucht. Es ist gut in organischen Lösungsmitteln löslich (beispielsweise Benzol, Toluol, Chlorbenzolen und anderen), es löst sich in Wasser unter rascher Zersetzung zu Kohlenstoffdioxid und Flusssäure, weshalb die organischen Lösemittel wasserfrei gemacht werden müssen, sollen diese zur Synthese oder zum Arbeiten mit Carbonylfluorid verwendet werden: EntstehungCarbonylfluorid entsteht meist als Zersetzungsprodukt fluorierter Kohlenwasserstoffe bei deren thermischer Zersetzung, beispielsweise aus Tetrafluormethan unter Anwesenheit von Wasser: Es kann auch aus Kohlenstoffmonoxid und Fluor synthetisiert werden: VerwendungEs ist keine großtechnische Verwendung für Carbonylfluorid bekannt; im Labormaßstab kann es für Fluor-Synthesen verwendet werden, da es sehr leicht unter Abgabe der Fluoratome Sauerstoff aufnimmt und zu Kohlenstoffdioxid weiter reagiert. Toxische WirkungCarbonylfluorid reizt bei inhalativer Aufnahme Haut, Augen und Atemwege. An Augen und Haut kommt es zu Schmerzen, Rötungen, schweren Verbrennungen und Sehbeeinträchtigungen durch Entziehen des Wassers aus dem Gewebe und zusätzlich durch den entstehenden Fluorwasserstoff. Bei einem Kontakt mit flüssigem Carbonylfluorid entstehen Erfrierungen. Nach längerer Aufnahme durch die Atemwege zeigt der Patient Halsschmerzen, Husten und Dyspnoe. Die Symptome können verzögert auftreten. Als schlimmste inhalatorische Folge kann ein toxisches Lungenödem auftreten. Dieses ist mit Cortison, auf jeden Fall auch präklinisch, zu therapieren. Quellen
Kategorien: Giftiger Stoff | Ätzender Stoff | Organofluorverbindung | Carbonsäurehalogenid | Gas |
||||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Carbonylfluorid aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | ||||||||||||||||||||||||||||||||||||||||||||||||