Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Charge-Transfer-KomplexeProdukt-Highlight
Charge-Transfer-KomplexeDie Farben vieler chemischer KomplexeViele chemische Komplexe sind farbig aufgrund der sogenannten Charge-Transfer-Absorption. Diese Charge-Transfer-Absorption ist die Absorption eines Lichtquants definierter Wellenlänge aus dem elektromagnetischen Spektrum. Dieser Lichtquant stellt nach der Gleichsetzung der Einsteinformel mit der Planckschen Quantelung der Energie 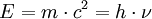 eine Energieform dar und kann innerhalb oder außerhalb des sichtbaren Bereichs des elektromagnetischen Spektrums liegen. Diese Energie wird dazu gebraucht, um Elektronen innerhalb der Komplexpartner hin und her zu verschieben. Nach der Orbital-Theorie befinden sich die unterschiedlichen Orbitale auch in unterschiedlichen Energieniveaus. Um ein Elektron von einem Energieniveau in ein anderes zu heben wird Energie benötigt. Die Charge-Transfer-Komplexe entnehmen den Energiewert aus dem elektromagnetischen Spektrum. Charge-Transfer-AbsorptionDie Energieabsorption aus dem elektromagnetischen Spektrum bedingt die Farbe des Komplexes. Wenn der Komplex im rot-violetten Bereich des sichtbaren Lichtes absorbiert, so erscheint der Komplex als bläulich-grün. Das menschliche Auge sieht somit die Komplementärfarbe. ElektronenübergängeIm Allgemeinen werden drei Elektronenübergänge innerhalb des Komplexes unterschieden. Übergang Ligand → MetallElektronladung (→ engl.: Charge) wird aus einem besetzten Molekülorbital (MO) des Liganden in ein niedrig liegendes, unbesetztes oder teilbesetztes MO des Metallatoms angeregt (→ engl. Transfer). Darunter fallen zum Beispiel die Thiocyanatoeisen(III)-Komplexe: Eisen mit der Oxidationszahl +III und einer Besetzung der d-Orbitale mit fünf Elektronen geht in Eisen mit der Oxidationszahl II und einer Besetzung der d-Orbitale mit sechs Elektronen über. Gleichzeitig wird der Thiocyanatligand zu einem Thiocyanat-Radikal oxidiert. Übergang Metall → MetallTritt ein bei Komplexen, die Metallatome unterschiedlicher Oxidationsstufe haben (e. g. Berliner Blau, Saphir). Diese Charge-Transfer-Komplexe haben meist sehr intensive Farben (im Fall des Berliner Blaus tiefblau). Übergang Metall → LigandEs erfolgt Elektronenanregung aus einem am Metall lokalisierten, besetzten MO (e. g. besetztes d-Orbital) in ein energetisch höher gelegenes leeres MO mit Ligandencharakter (e. g. in ein π * -Orbital gleicher Symmetrie). HalogenkomplexeStatt eines Metall-Kations können auch andere starke Elektronenakzeptoren als Zentralteilchen eines Komplexes fungieren. Hierzu eignen sich etwa Halogenmoleküle wie I2 und Br2, die mit den Molekülen bestimmter Lösungsmittel ein Lewis-Säure-Base-Addukt bilden können. Solche Substanzen heißen solvatochrom, da sie in Lösungsmitteln unterschiedlicher Polarität unterschiedliche Farbwirkungen erzeugen. Siehe auchKristallviolett, Tetranitromethan, Azulen, Kaliumpermanganat http://dc2.uni-bielefeld.de/dc2/tip/brenzkat.htm Kategorien: Organische Chemie | Spektroskopie |
|
| Dieser Artikel basiert auf dem Artikel Charge-Transfer-Komplexe aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |







