Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Drude-TheorieDie Drude-Theorie (auch Drude-Modell) ist eine klassische Beschreibung des Ladungstransports in Metallen oder verallgemeinert durch freie Elektronen in Festkörpern. Sie wurde 1900 von Paul Drude vorgestellt [1] [2], 1905 von Hendrik Antoon Lorentz erweitert und 1933 von Arnold Sommerfeld und Hans Bethe um die Ergebnisse der Quantentheorie ergänzt [3]. Produkt-Highlight
ModellbeschreibungIn dem Modell wird ein elektrischer Leiter als Ionenkristall betrachtet, in dem sich die Elektronen frei bewegen können. Verantwortlich für die Stromleitung sind demnach Elektronen, die sich in einem idealen Elektronengas befinden. Durch ein äußeres elektrisches Feld E erfahren die freien Elektronen im Leiter also eine Kraftwirkung Fel = eE und werden beschleunigt. Die Elektronen werden im Leitermaterial bei angelegter Spannung jedoch nicht kontinuierlich beschleunigt. Wäre dieses so, dürfte der Widerstand und die Stromstärke nicht konstant sein und das Ohmsche Gesetz würde somit nicht gelten. Es stellt sich nach kurzer Zeit ein Gleichgewicht ein, bei dem die mittlere Geschwindigkeit des Elektrons zur Feldstärke proportional ist. Das Drude-Modell erklärt diese Tatsache so: Das Elektron stößt mit einem Gitterion zusammen und wird abgebremst. Dieser Vorgang wird phänomenologisch durch eine mittlere Stoßzeit (Relaxationszeit) τ zwischen zwei Kollisionen beschrieben. Mit steigender Temperatur sinkt die mittlere Stoßzeit und erklärt damit die sinkende Leitfähigkeit der Metalle. Die Bewegungsgleichung hierfür lautet:
m: Elektronenmasse, v: Elektronengeschwindigkeit, vD:Driftgeschwindigkeit (e-Geschwindigkeit abzügl. der thermischen Geschwindigkeit), τ: Stoßzeit Für den stationären Zustand ( Mit der Ladungsträgerdichte n ist die Stromdichte j Die Leitfähigkeit σ ist: AnwendungsgebieteMit diesem Modell konnte erstmals das ohmsche Gesetz erklärt werden, wenn auch der mit diesem Modell berechnete Widerstandswert etwa sechs mal größer als der wahre (gemessene) Widerstandswert des jeweiligen Materials ist. Es hat aber auch noch weitere deutliche Schwächen: Das Drude-Modell steht mit seiner Annahme, alle Elektronen würden zum Strom beitragen, im Widerspruch zu den Aussagen des Pauli-Prinzips. Aber auch klassisch gesehen erzeugt diese Annahme einen Widerspruch: Aus der statistischen Thermodynamik folgt, dass alle Freiheitsgrade eines System (hier: Festkörper) im Mittel Grenzen des ModellsDas Modell sagt eine Proportionalität von Widerstand und Elektronengeschwindigkeit zur Wurzel aus der Temperatur voraus. Dieses ist in Wirklichkeit nicht gegeben. Des Weiteren kann überhaupt keine Aussage darüber getroffen werden, ob ein Material ein Leiter, Halbleiter oder ein Isolator ist. Letzteres ist ein Vorteil, da man die Theorie auch auf die freien Elektronen im Leitungsband eines Halbleiters anwenden kann. Abhilfe schafft die quantenmechanische Beschreibung des sommerfeldschen Modells [3]. Eine Erweiterung des Drude-Modells stellt das Drude-Lorentz-Modell dar. Dabei werden zusätzliche Adsorptionsmaxima beschreiben, die beispielsweise durch Bandübergänge verursacht werden. Mit dem Drude-Lorentz-Modell ist es möglich, die dielektrische Funktion einer Vielzahl von Materialien (auch Halbleiter und Isolatoren) zu beschreiben. Quellen
|
|
| Dieser Artikel basiert auf dem Artikel Drude-Theorie aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |





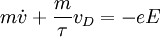 mit
mit
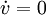 ) gilt:
) gilt:
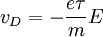
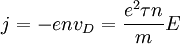
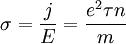
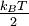 zu seiner
zu seiner 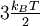 liefern.
Messungen haben aber gezeigt, dass der elektronische Beitrag zur Gesamtenergie etwa tausendmal kleiner ist.
liefern.
Messungen haben aber gezeigt, dass der elektronische Beitrag zur Gesamtenergie etwa tausendmal kleiner ist.


