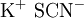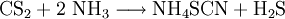Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Kaliumthiocyanat
Kaliumthiocyanat (KSCN) (auch: Kaliumrhodanid) ist ein Salz der Thiocyansäure (Rhodanwasserstoffsäure). Produkt-Highlight
EigenschaftenKaliumthiocyanat besteht bei Raumtemperatur aus Kristallen, die an der Luft langsam zerfließen. Es löst sich sehr gut in Wasser, wobei die Lösung stark abkühlt. Die Schmelztemperatur beträgt etwa 175 °C. Die Kristalle sind in Ethanol und Aceton gut löslich. HerstellungHergestellt werden kann Kaliumthiocyanat durch Zusammenschmelzen von Kaliumcyanid und Schwefel oder aus Ammoniumthiocyanat und Kalilauge. Ammoniumthiocyanat wiederum wird aus Schwefelkohlenstoff und Ammoniak unter Druck und erhöhter Temperatur hergestellt: VerwendungKaliumthiocyanat ist ein Nachweismittel für Fe3+-Ionen. Die Nachweiswirkung beruht auf einer Reaktion, in der Fe3+-Ionen mit den Thiocyanat-Ionen zum blutroten Eisenthiocyanat Fe(SCN)3 reagieren. Die darauf entstehende Färbung bezeichnet man umgangssprachlich als „Theaterblut“. Weitere Anwendungszwecke sind die Herstellung von Kältemischungen, Schädlingsbekämpfungsmitteln, Kunststoffen und Metallbeizen. Außerdem dient es in der Fotografie zum Tönen von Bildern. Quellen
Kategorien: Gesundheitsschädlicher Stoff | Kaliumverbindung | Thiocyanat | Pseudohalogen |
|||||||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Kaliumthiocyanat aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | |||||||||||||||||||||||||||||||||||||||||||||||||||