Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Moseleysches GesetzDas Moseleysche Gesetz (nach Henry Moseley) beschreibt die Lage der sogenannten Kα-Linien im Röntgenspektrum (das ist jene Linie, welche dem Übergang eines Elektrons von der L-Schale zur K-Schale entspricht). Produkt-HighlightIn einer allgemeineren Form kann man mit diesem Gesetz auch die Wellenlängen der übrigen Linien des Röntgenspektrums bestimmen. Die Wellenlänge λ der beim Elektronenübergang emittierten bzw. absorbierten charakteristischen Röntgenstrahlung ist abhängig von der Ordnungszahl Z des jeweiligen Elements und somit charakteristisch für ein bestimmtes Element. Es gilt:
Dabei ist:
Für den Übergang eines Elektrons von der zweiten (L-Schale) in die erste Schale (K-Schale), den sogenannten Kα-Übergang, gilt
|
| Dieser Artikel basiert auf dem Artikel Moseleysches_Gesetz aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |





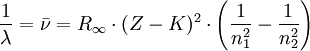
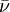 -
- 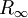 - Rydberg-Konstante (1,0973731534·107 m-1)
- Rydberg-Konstante (1,0973731534·107 m-1)
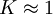 und die entsprechende Wellenzahl ist dann:
und die entsprechende Wellenzahl ist dann:
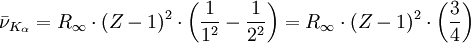 .
.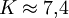 .
.

