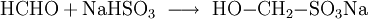Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Natriumhydrogensulfit
Natriumhydrogensulfit (NaHSO3), auch Natriumbisulfit, ist ein Natrium-Salz der Schwefeligen Säure. Im Gegensatz zum Natriumsulfit ist es jedoch nur als wässrige Lösung bekannt, nicht aber als Feststoff. Produkt-HighlightIm Handel befindet es sich als Lösung mit einem zwischen 37 und 50 % liegendem Gehalt an Natriumhydrogensulfit. Diese Lösungen weisen ätzende, reduzierende und stark bleichende Eigenschaften auf. Beim Aufkonzentrieren der wässrigen Lösung entsteht Natriumdisulfit (Na2S2O5) bzw. Natriumsulfit. Als Lebensmittelzusatzstoff E 222 findet Natriumhydrogensulfit Verwendung als Konservierungsmittel, Antioxidationsmittel und als Stabilisator in Lebensmitteln. Von Bedeutung ist die Additionsreaktion mit Formaldehyd unter Bildung des schwerlöslichen Formaldehyd-Natriumhydrogensulfit: Häufig wird diese Reaktion zur Aufreinigung von Aldehyden verwendet da sie unter basischen Bedingungen reversibel ist. Quellen
Kategorien: Gesundheitsschädlicher Stoff | Sulfit | Natriumverbindung |
||||||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Natriumhydrogensulfit aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | ||||||||||||||||||||||||||||||||||||||||||||||||||