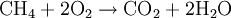Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Redox-PaarAls Redox-Paar werden in der Chemie zwei Stoffe in unterschiedlichen Zusammenhängen benannt. Einmal werden damit zwei Stoffe bezeichnet, die miteinander reagieren, aber auch zwei Stoffe, die wechselseitig ineinander übergehen. Produkt-HighlightElektrochemieAls Redox-Paar bezeichnet man in der Elektrochemie die Kombination einer reduzierten und einer oxidierten Form desselben Elements (siehe auch Oxidation und Reduktion). Solche Paare finden Verwendung in galvanischen Zellen zur Stromerzeugung oder in Messinstrumenten. Als Referenzpunkt für die Angabe von Elektrodenpotenzialen wurde die Kombination von H2 / 2H+ gewählt. Innerhalb dieses Redox-Paares ist H2 (Wasserstoff) die reduzierte Form und 2H+ (das Proton) die oxidierte Form des Wasserstoffes. RedoxreaktionAls Redoxpaar werden zwei chemische Substanzen bezeichnet, die bei einer Redoxreaktion miteinander reagieren. Einer der beiden Stoffe wird dabei oxidiert und der andere wird reduziert. Bei der Verbrennung von Methan mit Sauerstoff zu Kohlendioxid und Wasser bilden Methan und Sauerstoff ein Redoxpaar. Das Methan wird oxidiert und der Sauerstoff wird reduziert. Genauso kann man auch vom Kohlenstoff, der oxidiert wird und vom Sauerstoff, der reduziert wird, als Redoxpaar sprechen. Bei der gleichen Reaktion bilden auch Kohlendioxid und Wasser ein Redoxpaar, da auch die Rückreaktion (theoretisch) möglich ist. Kategorien: Chemische Reaktion | Elektrochemie |
| Dieser Artikel basiert auf dem Artikel Redox-Paar aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |