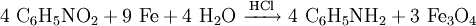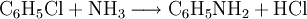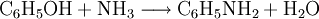Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Anilin
Anilin [aniˈliːn] (von arabisch an-nil „Indigopflanze“) ist eine farblose, leicht ölige Flüssigkeit mit süßlichem Geruch, die an der Luft leicht bräunlich wird. Es handelt sich um einen Benzolring mit einer Aminogruppe (–NH2) und damit um eine aromatische Verbindung. Mit Säuren versetzt bildet es Anilinsalze. Die basische Wirkung von Anilin wird durch den mesomeren Effekt verringert, da dieser zu einer geringeren Elektronendichte am sonst Protonen aufnehmenden NH2-Rest führt. Weiteres empfehlenswertes Fachwissen
GeschichtlichesAnilin wurde 1826 von Otto Unverdorben erstmals durch Kalkdestillation aus Indigo – einem blauen Farbstoff – hergestellt. Daher war es früher auch unter dem Namen Blauöl bekannt. Seit 1897 wird Anilin von der Badischen Anilin- und Soda-Fabrik (BASF) zur Synthese des vorher nur aus pflanzlichen Rohstoffen gewonnenen Farbstoffs Indigo eingesetzt (Heumann-Synthese). Schon vorher wurde Anilin in großem Maßstab hergestellt, etwa von der Agfa (Aktien-Gesellschaft für Anilin-Fabrikation) ab 1873. Eine bekannte Anwendung des Farbstoffes war Anilinleder. Auch in der Drucktechnik wurde Anilin verwendet, u. a. bekam der Flexodruck den auch heute noch verwendeten Beinamen Anilindruck, da erst durch das Anilin eine gute Druckqualität erzeugt werden konnte. HerstellungIn der Technik gewinnt man Anilin durch eine Reduktion von Nitrobenzol mit Eisen in Gegenwart von Salzsäure:
Anschließend wird mit Branntkalk (CaO) neutralisiert, und das Anilin zusammen mit dem Wasser abdestilliert. Es gibt noch andere Verfahren, zum Beispiel die Ammonolyse von Chlorbenzol oder Phenol: VerwendungEs dient in der chemischen Industrie in erster Linie als Ausgangsstoff für die Synthese von Farben und Kunstfasern, aber auch zur Herstellung von Kautschuk und Medikamenten. Giftigkeit von AnilinAnilin ist ein blutveränderndes Gift, welches Hämolyse auslösen kann und im Verdacht steht, krebsverursachend (karzinogen) zu sein. Da es über die Haut aufgenommen werden kann, ist es ein Kontaktgift. Siehe auch
Einzelnachweise
Literatur
SicherheitsdatenblätterSicherheitsdatenblätter verschiedener Hersteller in alphabetischer Reihenfolge für Anilin:
Kategorien: Giftiger Stoff | Umweltgefährlicher Stoff | Amin | Aromat |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Anilin aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||