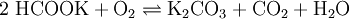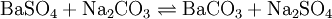Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Kaliumcarbonat
Kaliumcarbonat (Pottasche), K2CO3, das Kaliumsalz der Kohlensäure bildet ein weißes, hygroskopisches Pulver mit einer Schmelztemperatur von 891 °C und einer Dichte von 2,428 g·cm−3. Der Name Pottasche stammt von der alten Methode der Anreicherung von Kaliumcarbonat aus Holzasche mittels Lösung der Salze durch Auswaschen mit Wasser und anschließendem Eindampfen in Töpfen (Pötten). Der traditionelle Name stand auch Pate für den englischen Namen von Kalium: potassium. Weiteres empfehlenswertes Fachwissen
VerhaltenIn Wasser ist es sehr leicht und gut löslich (1120 g/l). Durch Hydrolyse reagiert die Lösung wegen der Bildung von Kaliumhydroxid alkalisch:
Mit Säuren entstehen unter Kohlendioxidentwicklung die entsprechenden Kaliumsalze. Bei Raumtemperatur kristallisiert es als Dihydrat aus der wässrigen Lösung. Vorkommen
GewinnungKaliumcarbonat lässt sich nicht wie Natriumcarbonat nach dem Ammoniak-Soda-Verfahren gewinnen, da das Zwischenprodukt Kaliumhydrogencarbonat (KHCO3) zu gut löslich ist.
Verwendung
Soda-Pottasche-AufschlussDer Soda-Pottasche-Aufschluss wird für schwerlösliche (Erdalkali-)Sulfate, hochgeglühte (saure oder amphotere) Oxide, Silicate und Ag-Halogenide verwendet; der Aufschluss findet in einer Na2CO3/K2CO3-Schmelze statt. ZrO2, Zr3(PO4)4, Al2O3, Cr2O3 und Fe2O3 werden nur teilweise gelöst. Für diesen Schmelzeaufschluss verwendet man Soda und Pottasche im Gemisch, weil damit eine Schmelzpunkterniedrigung gegenüber reinen Salzen zu erhalten ist (eutektische Legierung). Zudem drängt der enorme Carbonatüberschuss das Reaktionsgleichgewicht auf die Produktseite. Ein Beispiel für Sulfate: Quellen
Kategorien: Reizender Stoff | Carbonat | Kaliumverbindung |
|||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Kaliumcarbonat aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | |||||||||||||||||||||||||||||||||||||||||||||||






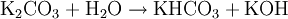 .
.