Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
KompressionsmodulDer Kompressionsmodul (Formelzeichen: K) ist eine intensive und stoffeigene physikalische Größe aus der Elastizitätslehre. Er beschreibt, welche allseitige Druckänderung nötig ist, um eine bestimmte Volumenänderung hervorzurufen. Die Eigenschaft von Stoffen, dass sie einer Komprimierung Widerstand entgegensetzen, hat ihre Ursache im Pauli-Prinzip. Weiteres empfehlenswertes Fachwissen
DefinitionDer Kompressionsmodul ist definiert als: Das negative Vorzeichen entsteht aus der Forderung, dass sich bei einem Druckzuwachs eine Abnahme der Größe dV/V ergibt, dabei aber K positiv bleiben soll. Die SI-Einheit des Kompressionsmoduls ist Pascal bzw. Newton/Quadratmeter. Der Kompressionsmodul ist eine Materialkonstante, die von der Temperatur und vom Druck abhängig ist. Der Zahlenwert stellt den Druck dar, bei dem das Volumen zu 0 wird, wenn der Kompressionsmodul bei höheren Drücken nicht ansteigen würde. Hierbei stehen die einzelnen Formelzeichen für folgende Größen:
Kompressionsmodul von Festkörpern mit isotropem MaterialverhaltenMan kann sie hierbei auch aus anderen Elastizitätskonstanten errechnen, unter Voraussetzung linear-elastischen Verhaltens und isotropen Materials: wobei:
Kompressibilität von Flüssigkeiten und GasenOft wird bei Gasen und Flüssigkeiten der Kehrwert des Kompressionsmoduls, die Kompressibilität (Formelzeichen: κ oder χ), auch Kompressibilitätskoeffizient, verwendet.
Lange wurde die Kompressibilität von Flüssigkeiten bezweifelt, bis sie John Canton 1761, Jacob Perkins 1820 und Hans Christian Oersted 1822 durch Messungen nachweisen konnten. Bei Gasen folgt die Kompressibilität dem Boyle-Mariotte-Gesetz. Beispiele
WasserDer Kompressionsmodul von Wasser beträgt bei einer Temperatur von 10 °C unter Normaldruck 2,08·109 Pa. Bezieht man die Kompressibilität des Wassers in die Berechnung des Drucks mit ein, ergibt sich mit der Kompressibilität
In 12.000 m Tiefe ergäbe sich hiermit bei einer Dichte von 1000 kg/m³ in 0 m Tiefe eine Abweichung des berechneten realen Drucks vom idealen von ca. 3,5 %. Hierbei bleiben jedoch weiterhin Temperatureffekte ebenso wie andere Einflüsse unberücksichtigt. NeutronensterneBei Neutronensternen sind unter dem Druck der Gravitation alle Atomhüllen zusammengebrochen und die Elektronen haben sich mit den Protonen der Atomkerne zu Neutronen verbunden. Neutronen sind die inkompressibelste Form der Materie, die bekannt ist. Ihr Kompressionsmodul liegt 20 Größenordnungen über dem von Diamanten. Siehe auch
Quellenangaben
Kategorien: Thermodynamik | Festigkeitslehre | Werkstoffeigenschaft |
|||||||||||||||
| Dieser Artikel basiert auf dem Artikel Kompressionsmodul aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | |||||||||||||||





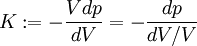
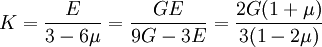
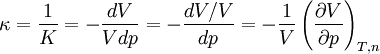 .
.
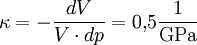 das folgende Diagramm:
das folgende Diagramm:


