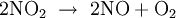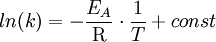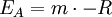Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
ArrheniusgraphAls Arrheniusgraphen (auch Arrheniusdarstellung oder -plot) bezeichnet man eine graphische Darstellung, bei der die Werte einer Messgröße (z.B. die Geschwindigkeitskonstante einer chemischen Reaktion) logarithmisch gegen den Kehrwert der Temperatur aufgetragen werden. Dadurch werden exponentiell von der Temperatur abhängige Werte auf eine Gerade abgebildet. Produkt-Highlight
Anwendung
Verwendet wird diese Art der Auftragung bei chemischen oder physikalischen Vorgängen, deren mathematische Beschreibung die Boltzmann-Konstante in der Form
oder
als Term enthält. In dieser Darstellung erscheint die Abhängigkeit der Messgröße von der Temperatur als Gerade, deren Steigung umgekehrt proportional zur Aktivierungsenergie EA ist. Bezogen auf die Geradengleichung entspricht die Steigung m dem Ausdruck Beispiele
Naturgesetze, die im Arrheniusplot linear dargestellt werden, sind die Temperaturabhängkeit der Reaktionsgeschwindigkeit (Arrhenius-Gleichung) und des Diffusionskoeffizienten in festen Stoffen. Nimmt man den natürlichen Logarithmus der Arrheniusgleichung: kann die Aktivierungsenergie nach aus der Geradensteigung errechnet werden. Auch wenn aufgrund von experimentellen Beobachtungen eine entsprechende Gesetzmäßigkeit vermutet wird, kann diese Annahme mit Hilfe der Arrheniusdarstellung beurteilt werden. Siehe auch
QuellenKategorien: Kinetik (Chemie) | Physikalische Chemie |
|||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Arrheniusgraph aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |





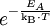 (einzelne Teilchen, siehe
(einzelne Teilchen, siehe 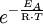 (makroskopische Ebene)
(makroskopische Ebene)
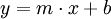
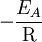 und der Kehrwert der Temperatur
und der Kehrwert der Temperatur 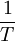 dem x-Wert.
dem x-Wert.