Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Cadmium(II)-chlorid
Cadmium(II)-chlorid ist das Chlorid des Cadmiums mit der Summenformel CdCl2. Es stellt den Prototyp einer AB2-Schichtstruktur mit kubisch-dichtester Kugelpackung dar. Produkt-Highlight
DarstellungWasserfreies Cadmium(II)-chlorid kann aus den Elementen durch Reaktion von erhitztem Cadmium mit Chlorgas gewonnen werden, alternativ kann auch Chlorwasserstoff eingesetzt werden: Anstelle des Cadmiums lassen sich auch Cadmium(II)-oxid oder Cadmium(II)-carbonat mit Salzsäure umsetzen. Die entstehenden Hydrate können dann mit Thionylchlorid entwässert werden. EigenschaftenCadmium(II)-chlorid bildet farblose, hygroskopische und sehr gut wasserlösliche Kristalle. Es kristallisiert in einer Schichtstruktur im trigonalen Kristallsystem (Raumgruppe 166, SicherheitshinweiseCadmium(II)-chlorid ist eine sehr giftige und umweltgefährliche Substanz, die karzinogen (R 45), mutagen (R 46) und reproduktionstoxisch (R 60/61) wirken kann. Eine akut toxische Wirkung besteht in einer starken Reizwirkung auf den Respirationstrakt nach dem Einatmen von Dämpfen oder Aerosolen bis zum Lungenödem. Eine chronische Vergiftung führt zur Schädigung von Nieren, Leber und Lungen. Optisches Merkmal einer Cadmiumvergiftung ist die Ausbildung eines gelben Saums an den Zahnhälsen durch sulfidische Cadmiumverbindungen. Für Mäuse wird eine LD50 von 4,6 mg/kg (intraperitoneal) angegeben. Darüber hinaus ist es extrem giftig für viele Wasserorganismen (Bakterien, Algen, Krustentiere). QuellenLiteratur
Kategorien: Giftiger Stoff | Umweltgefährlicher Stoff | Cadmiumverbindung | Chlorid | Rhomboedrisches Kristallsystem |
||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Cadmium(II)-chlorid aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | ||||||||||||||||||||||||||||||||||||||||||||||||||||







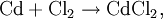
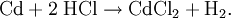
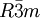 , a = 3,85 Å, c = 17,46 Å). Diese Struktur besteht aus einer
, a = 3,85 Å, c = 17,46 Å). Diese Struktur besteht aus einer 

