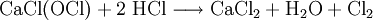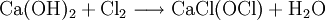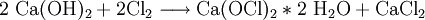Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Calciumhypochlorit
Calciumhypochlorit ist das Calciumsalz der Hypochlorigen Säure mit der chemischen Formel Ca(OCl)2. Wird es technisch hergestellt, entsteht meist ein gemischtes Chlorid-Hypochlorit-Salz mit der Formel CaCl(OCl) mit dem Namen Chlorkalk oder Bleichkalk. Herstellungsbedingt enthält er noch Anteile von Calciumhydroxid. Es wurde als erstes von 1798 von Charles Tennant hergestellt. Produkt-Highlight
EigenschaftenChlorkalk ist ein weißes, nach Chlor riechendes, wenig wasserlösliches Pulver. Chlorkalk entwickelt mit Säuren, sogar der Kohlensäure der Luft, Chlor. Beispiel anhand der Salzsäure: Beim Stehen und mit manchen Metalloxiden wird (besonders bei Lichteinwirkung) Sauerstoff frei gesetzt. HerstellungDie Gewinnung von Chlorkalk erfolgt durch Einwirken von Chlorgas auf gelöschten Kalk (Calciumhydroxid) in der Kälte: Möchte man reines Calciumhypochlorit herstellen, wird eine Calciumhydroxid-Suspension in der Weise chloriert, dass nur das Calciumchlorid in Lösung geht. VerwendungMedizinChlorkalk wurde zuerst durch den Mediziner Ignaz Semmelweis erfolgreich als Desinfektionsmittel eingesetzt; dadurch konnte die Sterblichkeit von Wöchnerinnen erheblich gesenkt werden. Allerdings greift Chlorkalk nicht nur Bakterien und Viren sondern auch die Haut an. Daher ist die Verträglichkeit nicht sehr gut und die Bereitschaft zur regelmäßigen Anwendung gering. Besser akzeptiert sind heute Händedesinfektionsmittel auf Alkoholbasis. Ferner wird es auch zur Dekontamination von diversen Kampfstoffen (Sarin, Senfgas ..) und als Algizid (Algenbekämpfungsmittel) eingesetzt. Technische VerwendungIn der Technik wird der Chlorkalk als Bleichmittel für Zellstoff, Papier und Textilien verwendet, wobei er aber aus Umweltschutzgründen durch andere chlorfreie Bleichverfahren verdrängt wird. Chemische IndustrieCalciumhypochlorit wird auch zur Herstellung von Chloroform, Schellack und bei der Cobaltgewinnung zur Trennung anderen Metallen verwendet. SicherheitshinweiseCalciumhypochlorit ist giftig (LD50 oral Ratte: 850 mg/kg[3]) und sollte kühl und trocken gelagert werden, da es zur Zersetzung unter Selbsterhitzung neigt. Quellen
Kategorien: Ätzender Stoff | Brandfördernder Stoff | Umweltgefährlicher Stoff | Chlorid | Hypochlorit | Calciumverbindung |
|||||||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Calciumhypochlorit aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | |||||||||||||||||||||||||||||||||||||||||||||||||||