Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
DiamantstrukturAls Diamantstruktur (auch Diamantgitter oder Diamanttyp) bezeichnet man eine bestimmte Kristallstruktur, also ein bestimmtes Anordnungsmuster der Atome. Der Name rührt daher, dass das erste entdeckte Beispiel der Diamant war, eine Modifikation des Kohlenstoffs , die im kubischen Kristallsystem kristallisiert. Andere Elemente der 4. Hauptgruppe (vierwertiges Element; Atome mit 4 Valenzelektronen) können ebenfalls in dieser Struktur kristallisieren. Dazu gehören die Halbleiter α-Zinn, Silicium und Germanium sowie Silicium-Germanium-Legierungen in beliebigen Mischungsverhältnissen . Produkt-Highlight
Aufbau
Das Diamantgitter besteht aus zwei sich gegenseitig durchdringenden kubisch flächenzentrierten (engl. face-centered cubic, fcc) Gittern. Jedes Kohlenstoffatom ist gleichwertig mit vier Nachbaratomen kovalent gebunden. Die Diamantstruktur entspricht damit dem Zinkblende-Gitter (ZnS) mit dem Unterschied, dass jedes Atom mit 4 Atomen des gleichen Elements (beim Diamant C-Atome) verbunden ist. Der Grund dafür ist die Hybridisierung der Orbitale der äußersten Schale des Grundzustandes (Kohlenstoff: 1s22s22p2) zu vier sp3-Hybridorbitalen (1s24sp3). Diese vier Orbitale sind aufgrund der elektromagnetischen Abstoßung mit größtmöglichem Abstand bzw. Winkel (109,5°) zueinander symmetrisch im Raum orientiert, sie zeigen in die Ecken eines gedachten Tetraeders. Vereinfachende zweidimensionale Abbildungen von Gittern mit vierwertigen Elementen zeigen ein gewöhnliches zweidimensionales Gittermuster. Im dreidimensionalen Raum nehmen die vier Valenzelektronen jedoch eine Position ein, die den vier Ecken eines Tetraeders entspricht, wobei der Atomkern im Mittelpunkt des Tetraeders liegt. In 2D-Darstellungen der 3D-Struktur von Diamanten wird das Atom gezeichnet, von dem aus sich die vier Ecken des Tetraeders in vier Bindungen (Valenzen) ausstrecken. Bei Aufsicht auf diese Tetrader der Diamantstruktur liegen drei Valenzen an den drei Ecken eines gleichseitigen Dreieckes und berühren drei benachbachbarte Atome, die in einer gemeinsamen Ebene liegen. Die vierte Valenz liegt in der Mitte des Dreieckes und berührt ein viertes benachbartes Atom in einer anderen Ebene – näher zum Betrachter hin bzw. weiter vom Betrachter weg. In der Diamantstruktur sind die Tetraeder abwechselnd so gedreht, dass die vierte Valenz zum Betrachter zeigt bzw. von ihm weg. Kristallografische RaumgruppeDie Diamantstruktur wird in der kristallographischen Raumgruppe
Stereografische ProjektionDie Stereografische Projektion der Diamantstruktur zeigt eine dreifache Symmetrie (Kristallebene [111] ) EigenschaftenWie erwähnt kristallisieren die typischen vierwertigen Halbleiter wie Silicium und Germanium in der Diamantstruktur. Durch die starken kovalenten Bindungen existieren keine freien Elektronen und die Materialien weisen bei T = 0 K (Temperatur am absoluten Nullpunkt) abgesättigte Valenzen, d. h. vollbesetzte Valenzbänder (VB), auf. Das Leitungsband (LB) ist hingegen völlig leer. Reine Halbleiter ohne Kristallbaufehler sind daher bei T = 0 K Isolatoren, denn es stehen keine Ladungsträger (Elektronen oder Defektelektronen) für den Stromtransport zur Verfügung. Die Bandstruktur von Materialien mit Diamantstruktur weist meist eine Energielücke (Bandlücke) auf. Diese nimmt je nach Element unterschiedliche Werte an (Eg,Diamant = 5,4 eV, Eg,Silicium= 1,1 eV). Bei den geringen Werten für die Energielücke bei Silicium und Germanium (0,67 eV) reicht bereits die Wärmeenergie bei Raumtemperatur aus, um Elektronen aus dem Valenzband in das Leitungsband zu heben. Die Elektronen im LB und die zurückbleibenden Defektelektronen im VB können nun unter dem Einfluss eines von außen angelegten elektrischen Feldes den elektrischen Stromleiten. Dieser Übergang der Elektronen vom Valenzband zum Leitungsband kann auch durch Photonen verursacht werden (photoelektrischer Effekt). Außerdem kann die Energielücke durch gezieltes Verunreinigen (Dotierung) und den damit entstehenden Haftstellen (ortsgebunden) verringert und somit die Leitfähigkeit erhöht werden (Störstellenleitung). Da beim Diamant nur vier der acht tetraedischen Lücken von Kohlenstoffatomen besetzt sind, ist das Gitter relativ stark aufgeweitet. Die Packungsdichte des Diamantgitters – nicht nur beim Diamant − ist somit vergleichsweise klein, nur etwa 34 Prozent des verfügbaren Gittervolumens sind besetzt. Die besondere Härte von Diamant lässt sich mit dem Gittermodell nicht erklären, sie ist eine Folge der besonders festen und gerichteten kovalenten Bindungen, die die tetraedischen sp³-Orbitale des Kohlenstoffs eingehen. Siehe auchBravais-Gitter | Kristallsystem | Tetraederlücke Kategorien: Kristallstrukturtyp | Kubisches Kristallsystem |
|
| Dieser Artikel basiert auf dem Artikel Diamantstruktur aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |





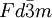 beschrieben. Es handelt sich also um eine kubische Kristallstruktur.
beschrieben. Es handelt sich also um eine kubische Kristallstruktur.
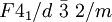 . F bedeutet, dass das
. F bedeutet, dass das 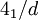 bedeutet eine 41-Schraubenachse parallel der kristallographischen a-Achse (Drehung um 90° und Verschiebung (Translation) um 1/4 in Richtung der a-Achse), die 41-Schraubenachse steht weiterhin senkrecht auf einer Gleitspiegelebene (d). Entlang der Raumdiagonalen der
bedeutet eine 41-Schraubenachse parallel der kristallographischen a-Achse (Drehung um 90° und Verschiebung (Translation) um 1/4 in Richtung der a-Achse), die 41-Schraubenachse steht weiterhin senkrecht auf einer Gleitspiegelebene (d). Entlang der Raumdiagonalen der 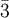 . Parallel zu den Winkelhalbierenden der Flächen der Elementarzelle befinden sich zweizählige Drehachsen (2) und senkrecht dazu Spiegelebenen (m). (Siehe dazu auch:
. Parallel zu den Winkelhalbierenden der Flächen der Elementarzelle befinden sich zweizählige Drehachsen (2) und senkrecht dazu Spiegelebenen (m). (Siehe dazu auch: 

