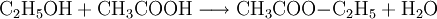Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Ethylacetat
Ethylacetat (UN-Nummer: 1173) ist ein charakteristisch „nach Klebstoff“ riechendes Lösungsmittel, das in der chemischen Industrie und in Laboratorien oft verwendet wird. Ethylacetat ist der Ester aus Essigsäure und Ethanol, daher wird er auch Essigsäureethylester oder kurz Essigester (EE) genannt. Ein veralteter Name ist Essigäther. Es ist eine farblose Flüssigkeit. Der Brechungsindex beträgt 1,370 (bei 20°C), der Flammpunkt liegt bei −4 °C. Produkt-Highlight
HerstellungEine der chemischen großtechnischen Herstellungsverfahren beruht auf der Umsetzung von Ethanol mit Essigsäure: Diese Gleichgewichtsreaktion wird nach dem Prinzip von Le Chatelier (Massenwirkungsgesetz) durch fortlaufende Abtrennung des entstehenden Wassers kontinuierlich auf die Seite der Produkte verlagert. In Ländern, in denen Acetaldehyd ausreichend zur Verfügung steht, wird die Verbindung großtechnisch katalytisch aus diesem Vorprodukt hergestellt. VerwendungEthylacetat ist ein vielseitig einsetzbares Lösemittel. Ethylacetat wird auch zur Extraktion von Antibiotika und zur Aromatisierung von Limonaden, Bonbons und Arzneimitteln verwendet. In Rum und einigen anderen Spirituosen ist es von Natur aus in geringen Mengen vorhanden. Auch im Wein kommt es in geringen Mengen vor, besonders wenn die Trauben durch Hagel oder Fäulnis geschädigt wurden; es verursacht dann einen Lösungsmittelton im Wein. In Klebstoffen ist es eines der am häufigsten eingesetzten Lösungsmittel. In hoher Konzentration ist es ein Suchtgift, welches von sogenannten "Schnüfflern" verwendet wird, um sich zu berauschen. Dies kann schwere Hirnschäden verursachen. Aufgrund seiner starken Lösungskraft findet Ethylacetat auch als Bestandteil von Nagellackentferner Verwendung. In der Entomologie ist es das am häufigsten eingesetzte Tötungsmittel bei der Präparation von Insekten. Wiki/Weblinks
SicherheitsdatenblätterSicherheitsdatenblätter für Ethylacetat verschiedener Hersteller in alphabetischer Reihenfolge:
Kategorien: Feuergefährlicher Stoff | Reizender Stoff | Carbonsäureester |
||||||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Ethylacetat aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | ||||||||||||||||||||||||||||||||||||||||||||||||||