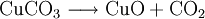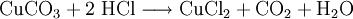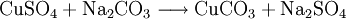Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Kupfer(II)-carbonat
Kupfer(II)-carbonat ist das Kupfersalz der Kohlensäure.
Produkt-Highlight
EigenschaftenWasserfreies Kupfer(II)-carbonat ist ein geruchsloses hellblaues Pulver, das Monohydrat hingegen ist dunkelgrün. Es ist in Wasser unlöslich und zersetzt sich ab 140°C zu Kupfer(II)-oxid und Kohlenstoffdioxid: Beim Lösen in Säuren entsteht Kohlenstoffdioxid: DarstellungKupfer(II)-carbonat wird im Labor durch mischen einer Kupfersulfatlösung und einer Natriumcarbonatlösung hergestellt: Da Kupfer(II)-carbonat in Wasser unlöslich ist, fällt es aus der Lösung aus und kann abfiltriert werden. VerwendungKupfer(II)-carbonat wird zur Herstellung vieler Kupferverbindungen, wie Kupfersulfat und Kupferoxid verwendet.
VorkommenKupfer(II)-carbonat kommt in der Natur als Malachit vor.
Quellen
Kategorien: Gesundheitsschädlicher Stoff | Kupferverbindung | Carbonat |
||||||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Kupfer(II)-carbonat aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | ||||||||||||||||||||||||||||||||||||||||||||||||||