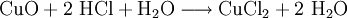Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Kupfer(II)-chlorid Dihydrat
Produkt-HighlightWenn Kupfer(II)-chlorid Dihydrat erhitzt wird, gibt es bei knapp über 100°C sein Kristallwasser ab. Wässrige Lösungen sind in hoher Konzentration braun, die beim Verdünnen grün und bei stärkerer Verdünnung blassblau werden. DarstellungIm Labor kann man Kupferchlorid durch Lösen von Kupfer(II)-oxid in Salzsäure herstellen.
Technisch wird es durch Chlorierung von Kupferblech gewonnen. VerwendungKupferchlorid wird in der Pyrotechnik zur Erzeugung grüner Flammen eingesetzt. Außerdem wird das Salz als Katalysator bei organischen Synthesen benutzt. Bei der Kupferätzung (in einer Mischung mit Salzsäure) und in der Photographie wird es zum Ausbleichen von Negativen verwendet. Quellen
Kategorien: Gesundheitsschädlicher Stoff | Umweltgefährlicher Stoff | Kupferverbindung | Chlorid |
|||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Kupfer(II)-chlorid_Dihydrat aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | |||||||||||||||||||||||||||||||||||||||||||