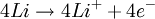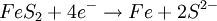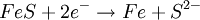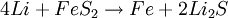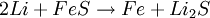Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Lithium-Eisensulfid-BatterieDie Lithium-Eisensulfid-Batterie beziehungsweise Lithium-Eisensulfid-Zelle ist ein galvanisches Element und zählt zu den nicht wiederaufladbaren Lithium-Batterien (Primärbatterien). Die Anode (positive Elektrode) besteht aus metallischem Lithium und die Kathode (negative Elektrode) besteht aus Eisensulfid. Der Elektrolyt ist eine Lösung von Lithiumiodid (LiI) in einem Gemisch aus organischen Lösungsmitteln. Die Nennspannung einer Zelle beträgt 1,5 V, deshalb kann sie als Ersatz für andere verbreitete Gerätebatterien (Alkali-Mangan-Batterie, Zink-Kohle-Batterie) dienen. Vorteile gegenüber diesen sind höhere Kapazität (insbesondere bei Entladungen mit hohen Strömen und bei tiefen Temperaturen) und längere Lagerfähigkeit. Nachteil ist der deutlich höhere Preis, der durch die aufwändigere Konstruktion bedingt ist. 1979 wurden Lithium-Eisensulfid-Knopfzellen als preisgünstige Alternative zu Silberoxid-Zink-Batterien für Uhren vorgestellt. Aufgrund des fallenden Preises für Silber wurden erstere jedoch bald wieder vom Markt genommen. Rundzellen der Baugrößen Mignon (AA) und Micro (AAA) sind seit 1992 beziehungsweise 2004 erhältlich. Prototypen von Hochtemperatur-Lithium-Eisensulfid-Akkumulatoren zur Anwendung als Traktionsbatterie wurden in den 1970er/1980er Jahren am Argonne National Laboratory (Illinois, USA) entwickelt. Produkt-Highlight
ElektrochemieIn der Lithium-Eisensulfid-Zelle liefern die Oxidation von Lithium und die Reduktion von Eisensulfid die elektrische Energie. Die theoretische Kapazität von Lithium beträgt 3,86 Ah/g, von Eisensulfid (FeS) 0,61 Ah/g und von Eisendisulfid (FeS2) 0,89 Ah/g. Die in der Zelle ablaufenden Reaktionen sind komplex und werden im folgenden vereinfacht dargestellt. Beim Entladen wird in der Anode metallisches Lithium (Li) zu Lithium-Ionen oxidiert. Die Oxidationszahl von Lithium erhöht sich dabei von ±0 auf +I. Anodenreaktion: Beim Entladen wird in der Kathode Eisendisulfid (FeS2) zu Eisen (Fe) und Sulfid-Ionen (S2-) reduziert. Die Oxidationszahl von Eisen verringert sich dabei von +2 zu ±0, die (formale) Oxidationszahl von Schwefel verringert sich dabei von -I im Disulfid-Ion (S22-) auf -II im Sulfid-Ion (S2-). Alternativ kann auch Eisensulfid (FeS) als Kathodenmaterial verwendet werden. In diesem Fall wird bei der Entladung nur Eisensulfid zu Eisen reduziert. Die Oxidationszahl von Eisen verringert sich dabei von +2 zu +/-0. In der Praxis wird nur FeS2 als Kathodenmaterial verwendet, da die Zellspannung und Kapazität in diesem Fall höher sind. Kathodenreaktion (FeS2): Kathodenreaktion (FeS): Die Gesamtreaktion kann wie folgt dargestellt werden: Gesamtreaktion (Li-FeS2): Gesamtreaktion (Li-FeS): Als Elektrolyt wird ein Gemisch verschiedener organischer Lösungsmittel (1,3-Dioxolan, 1,2-Dimethoxyethan) mit Lithiumiodid (LiI) verwendet. AufbauDie im Handel erhältlichen zylindrischen Li-FeS2Rundzellen in den Baugrößen Micro (AAA) mit der IEC-Bezeichnung FR03 und Mignon (AA) mit der IEC-Bezeichnung FR6 sind sogenannte Wickelzellen. Das heißt, die Elektroden sind Folien und werden mit dem dazwischenliegenden mikroporösen Separator aus Polyethylen oder Polypropylen zu einer Rolle gewickelt. Die Anodenfolie besteht aus Lithium und die Kathodenfolie aus einem mit Eisendisulfid beschichteten metallischen Träger. Zum Schutz gegen einen externen Kurzschluss ist die Zelle mit einem Thermoschalter (PTC-Widerstand) ausgestattet. Aufgrund des hohen Stromflusses beim Kurzschluss erwärmt sich die Zelle stark. Wenn die Aktivierungstemperatur des Thermoschalters erreicht wird, nimmt sein Widerstand zu, und der Stromfluss (und damit die Wärmeentwicklung) wird begrenzt. EigenschaftenDie Nennspannung der Lithium-Eisensulfid-Zelle beträgt 1,5 V. Die Leerlaufspannung liegt bei etwa 1,8 V. Die Lastspannung ist im Vergleich zu Alkali-Mangan-Zellen bei gleicher Belastung höher, und die Entladekennline verläuft flacher. Dadurch erklärt sich die höhere Belastbarkeit und Kapazität von Lithium-Eisensulfid-Zellen im Vergleich zu Alkali-Mangan-Zellen bei Einsatz in Anwendungen mit hohem Strom- beziehungsweise Leistungsbedarf (beispielsweise Digitalkameras und Blitzgeräten). Je kleiner der Strom- beziehungsweise Leistungsbedarf der Anwendung, desto geringer wird der Vorteil der Lithium-Eisensulfid-Zelle. Lithium-Eisendisulfid-Zellen können im Temperaturbereich von etwa -40°C bis 60°C betrieben werden. Wie bei allen Batteriensystemen wird die tatsächlich entnehmbare Kapazität mit steigender Temperatur höher. Die Lithium-Eisensulfid-Batterie zeichnet sich durch sehr gute Lagerfähigkeit aus (laut Herstellerangaben 10−15 Jahre). Siehe auch
Literatur
|
|
| Dieser Artikel basiert auf dem Artikel Lithium-Eisensulfid-Batterie aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |