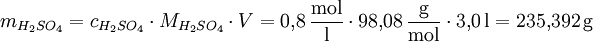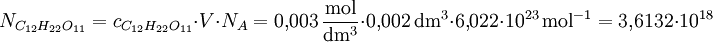Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
MolaritätUnter der Molarität (veralteter Begriff) oder Stoffmengenkonzentration (Formelzeichen: c) versteht man den Quotienten aus der Stoffmenge (n) eines gelösten Stoffes X und dem Volumen (V) der Lösung. Sie kann in der Einheit Mol pro Liter angegeben werden: Produkt-HighlightBei Kenntnis der molaren Masse kann aus der Stoffmengenkonzentration die Massenkonzentration errechnet werden, mit Hilfe der Avogadro-Konstante kann aus der Stoffmengenkonzentration die Teilchenzahlkonzentration ermittelt werden. Früher wurde das Symbol "M" für die Maßeinheit mol/L verwendet und auch zusammen mit SI-Vorsätzen benutzt; diese Schreibweise ist jedoch nicht mit dem Internationalen Einheitensystem (SI) verträglich. Die Molarität (Stoffmengenkonzentrationen) darf nicht mit der Molalität verwechselt werden! Im angelsächsischen Schrifttum ist mit „concentration“ stets die Stoffmengenkonzentration gemeint. Schreibweise mit AdjektivMit einer 2,5-molaren (veraltete Darstellungsweise auch: 2,5 M) wässrigen Schwefelsäure ist eine solche gemeint, die 2,5 Mol Schwefelsäure-Moleküle in 1 Liter Lösung einer bestimmten Temperatur enthält; hierbei ist die übliche Einheit mol/l zugrunde gelegt; RechenbeispieleIn einer 0,8-molaren (0,8 M) Schwefelsäurelösung (molare Masse von Schwefelsäure: 98,08 g/mol) sind pro Liter Lösung 0,8 mol H2SO4 enthalten. Die entsprechende Masse an H2SO4 für ein Volumen V = 3 Liter einer solchen Schwefelsäure beträgt: Die Teilchenzahl N einer 3-millimolaren (3 mM) Lösung von Rohrzucker in Wasser bei einem Lösungsvolumen V = 2 Kubikzentimeter, wobei NA (Avogadro-Konstante) die Anzahl der Teilchen pro Mol angibt, beträgt: Siehe auch
Kategorien: Physikalische Chemie | Chemische Größe |
| Dieser Artikel basiert auf dem Artikel Molarität aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |


![c_X = \frac {n_X}{V} \qquad [c_X] = 1 \frac{\rm mol}{\rm l}](images/math/7/5/8/75881faf16568e7e96f6da8f5cd98e23.png)