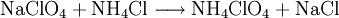Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Natriumperchlorat
Natriumperchlorat ist das Natriumsalz der Perchlorsäure mit der Summenformel NaClO4. Als Arzneistoff wird es zur Behandlung der Schilddrüsenüberfunktion eingesetzt. Produkt-Highlight
Gewinnung und DarstellungDie industrielle Herstellung erfolgt in sogenannten Perchloratzellen. Dabei wird in Wasser gelöstes Natriumchlorid elektrolytisch zu Natriumperchlorat oxidiert. EigenschaftenNatriumperchlorat bildet hygroskopische farblose Kristalle. Seine Bildungswärme beträgt −382,75 kJ mol−1. VerwendungDer Hauptverwendungszweck von allen Perchloratsalzen ist ihre Nutzung als Sauerstofflieferant in Festtreibstoffen. Anstelle von Natriumperchlorat wird jedoch meist Ammoniumperchlorat verwendet, das industriell in einer Ionenaustauschreaktion durch Umsetzung des Natriumsalzes mit einem Ammoniumsalz hergestellt wird: Durch die verschiedenen Löslichkeiten der Salze lassen sich diese leicht trennen. Das entstandene Natriumchlorid lässt sich wiederum als Ausgangsprodukt für die Perchloratzelle verwenden. Natriumperchlorat hemmt kompetitiv die Iodaufnahme in die Schilddrüse. Es wurde daher früher zur Behandlung der Hyperthyreose eingesetzt. Die einzige heutige Anwendung von Natriumperchlorat ist bei Verabreichung iodhaltiger Kontrastmittel als Zusatzmittel gegeben. Vor allem wenn 123I-markierte Radiopharmaka zum Einsatz kommen wird Natriumperchlorat verabreicht, um die Strahlenbelastung der Schilddrüse gering zu halten. SicherheitshinweiseNatriumperchlorat ist brandfördernd. Bei Verunreinung oder im Gemisch mit anderen Substanzen ist akute Brand- oder Explosionsgefahr gegeben. Bei der Zersetzung bilden sich giftige, aggressive Dämpfe. Quellen
Kategorien: Brandfördernder Stoff | Gesundheitsschädlicher Stoff | Perchlorat | Natriumverbindung |
||||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Natriumperchlorat aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | ||||||||||||||||||||||||||||||||||||||||||||||||