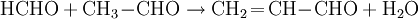Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Propenal
Produkt-Highlight
SynthesePropenal (auch Acrolein, Acrylaldehyd, 2-Propenal bzw. Prop-2-enal oder Aqualin) ist ein klarer flüssiger Stoff, der durch partielle Oxidation von Propen oder durch Reaktion von Acetaldehyd mit Formaldehyd gewonnen werden kann: Zudem ist Propenal unerwünschtes Produkt vieler Oxidationsreaktionen diverser organischer Verbindungen. Glycerol reagiert schon bei Temperaturen ab 200 °C unter Dehydratisierung zu Acrolein. Beim Verbrennen organischer Nutzchemikalien (Druckertinte, Pflanzenöle, Biodiesel uvm.) entstehen Propenaldämpfe. Acrolein entsteht auch beim Überhitzen pflanzlicher und tierischer Fette, zum Beispiel beim Frittieren. Dieser Prozess wird durch das Vorhandensein von Wasser und Säuren deutlich erleichtert. Dabei wird das Fett (Triglycerid) zunächst in seine Bestandteile Glycerol und Fettsäuren zerlegt (Verseifung). Das Glycerol wird dann weiter zu Acrolein dehydratisiert (nicht dehydriert). Die technische Herstellung in der chemischen Industrie erfolgt weitestgehend über die Gasphasenoxidation von Propan oder Propen in Gegenwart geeigneter heterogener Katalysatoren. Diese Partialoxidation am festen Kontakt (synonym zu „heterogener Katalysator“) erfolgt mit Luft als Oxidationsmittel bei Temperaturen um 330-360 °C wobei Rohrbündelreaktoren eingesetzt werden, die die stark exotherme Reaktion mit Salzbädern kühlen. Es wird nur eine relativ verdünnte Mischung von Propen mit Luft (meist noch in Gegenwart von Wasserdampf) eingesetzt, um die Bildung explosionsfähiger Gemische zu vermeiden. Die mit modernen Katalysatoren erzielbaren Ausbeuten betragen zwischen 80-85 % bezüglich Propen, als Nebenprodukte entstehen 4-8 % Acrylsäure und 4-6 % Kohlenmonoxid und Kohlendioxid neben nicht umgesetzten Propen. Problematisch ist die Quenchung und Isolierung des Acroleins vor der weiteren Verwendung als Rohstoff für die Synthese von Methionin, Glutaraldehyd oder diversen Riechstoffen. Bei der Isolierung kommt es zu Polymerisation von Acrolein und anderen aktiven Nebenkomponenten (im besonderen Acrylsäureester), die zum Abstellen der Anlage zwingen. Heute wird Acrolein von der Fa. Degussa an den Standorten Antwerpen, Mobile (Alabama) und Wesseling mit einer Gesamtkapazität von ca. 180 ktons p.a. (= per annum) hergestellt, der größere Teil wird direkt vor Ort zur Herstellung der Aminosäure Methionin verwendet (sog. „Captive Use“). Weitere größere Produktionsanlagen werden von der französischen Adisseo (vormals Rhone Poulenc, dann Aventis Animale Nutrition) am Standort Les Roches de Condrieu betrieben, hier kann man von einer Kapazität von etwa 75-80 ktons p.a. ausgehen, die ebenfalls mehr oder weniger exklusiv für die Synthese von Methionin Verwendung findet. Die Fa. Arkema (vormals Elf Aquitaine, dann Atofina) hat die Produktion von 30 ktons p.a. Acrolein am Standort Pierre Benite im Frühjahr 2004 eingestellt, als unmittelbare Folge einer großen Explosion bei Lyon, was eine wesentliche Diskussion über Gefahrguttransporte in Frankreich ausgelöst hat; Arkema betreibt seit 2005 am Standort Beaumont eine Acroleinanlage mit einer Kapazität von ca. 36-38 ktons p.a., die dort erzeugten Mengen werden aber direkt durch Umsetzung mit Methylmercaptan zu einem Methioninvorprodukt umgesetzt („captive use“). Die Fa. Sumitomo betreibt eine weitere Anlage in Japan (Standort Ehime) mit etwa 35-40 ktons Kapazität p.a., die Fa. DOW produziert am Standort Taft Acrolein, wobei hier widersprüchliche Angaben zur Kapazität existieren, geschätzt werden ca. 80-90 ktons p.a.. In zunehmenden Maße wird versucht, Acrolein nicht mehr aus Propan oder Propen herzustellen. Propan und Propen werden aus Erdgas und Erdöl gewonnen. Der Preis für fossile Rohstoffe wird auf absehbare Zeit immer mehr ansteigen. Deshalb versuchen viele Hersteller, Acrolein durch Deyhdratisierung von Glycerol (=Glycerin) zu produzieren. Glycerol ist aus Biodiesel billig erhältlich und nicht an den Rohölpreis gekoppelt. Im Moment sind derartige Verfahren noch nicht wirtschaftlich, da Rohglycerol aus Biodiesel zu unrein für die direkte Umsetzung ist. Fortschritte auf diesem Gebiet sind für die nächsten 5 bis 10 Jahre (Stand: April 2007) zu erwarten. EigenschaftenDie geringe Größe des Propenals, die Aldehydgruppe sowie die vorhandene Doppelbindung sorgen für eine hohe Reaktivität des Moleküls. Propenal zerfällt beim Erhitzen zu Methan und Kohlenstoffmonoxid. ReaktionsverhaltenAufgrund der vorhandenen C=C-Doppelbindung kann Propenal leicht polymerisieren. Propenal wird auch zu Glycerin umgesetzt. Die Aldehydgruppe kann an Proteine binden. Daher wird Propanal, ähnlich wie Formalin, in der Elektronenmikroskopie zur Fixierung eingesetzt. Der Vorteil liegt in der im Vergleich mit anderen Aldehyden besonders kurzen Reaktionszeit. GefahrenPropenal ist sehr giftig und zudem auch ein starkes Umweltgift. Es ist ein starker Wasser- und Meeresschadstoff und sehr schädlich für Fische. Nach der MAK-Kommission der DFG ist Propenal krebserzeugend (Kategorie 3B). Darunter fallen Stoffe, die wegen erwiesener/möglicher krebserzeugender Wirkung Anlass zur Besorgnis geben. Propenal ist sehr leicht entzündlich und kann mit der Luft explosionsfähige Gemische bilden. Es bildet durch Autoxidation Peroxide, welche vor Nutzung des Propenals zu entfernen sind. Kategorien: Giftiger Stoff | Feuergefährlicher Stoff | Umweltgefährlicher Stoff | Aldehyd | Alken |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Propenal aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||