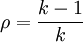Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
ReaktivitätDer Begriff Reaktivität wird allgemein als Maß zur Beschreibung von Reaktionen verwendet, und zwar in unterschiedlicher Bedeutung in der Soziologie, in der Chemie, in der Physik (Kerntechnik) und in der Medizin (Pathophysiologie und Radiologie). Produkt-Highlight
SozialwissenschaftenBei den Methoden der empirischen Sozialforschung werden reaktive Verfahren und nichtreaktive Verfahren unterschieden. Reaktive Verfahren sind Methoden, bei denen der Erhebungsleiter teilnimmt. Nichtreaktive (verdeckte) Verfahren sind Methoden, bei denen der Erhebungsleiter nicht teilnimmt. siehe Reaktivität (Sozialwissenschaften) ChemieIn der Chemie ist Reaktivität die Fähigkeit eines Stoffes, eine chemische Reaktion einzugehen. Sie ist weder eine thermodynamische noch eine kinetische Größe, sondern eine qualitative Bezeichnung für die Stabilität oder Reaktionsfreudigkeit einer Substanz. Beispiele: 1. Legt man elementares Kalium an normale Luft, reagiert es z. T. unter Entzündung mit der Luftfeuchtigkeit. Das Kalium hat eine hohe Reaktivität, ist reaktionsfreudig. 2. Legt man es unter Argon oder Petrolether, erfolgt keine merkliche Reaktion. Unter Argon hat Kalium eine geringe Reaktivität. Möchte man die Reaktivität über physikalische Größen beschreiben, hängt sie thermodynamisch von der freien Enthalpie oder Gibbs-Energie ab. Diese gibt vereinfacht ausgedrückt an, wie viel Energie einem Stoff zur Freisetzung zur Verfügung steht. Dies ist eine Eigenschaft des Stoffes. Die der Reaktivität entsprechende kinetische Größe bei einer Reaktion heißt Aktivierungsenergie. Dies ist grob gesagt die Energie, die aufgebracht werden muss, um eine Reaktion „in Gang zu bringen“ und bestimmt damit die Reaktionsgeschwindigkeit. Also beantwortet sie die Frage: „In welcher Zeit wird die Energie bei dieser Reaktion abgegeben?“. PhysikDie Reaktivität ist in der Kerntechnik ein Maß für die Abweichung des Multiplikationsfaktors k vom Wert k = 1. Sie beschreibt damit ebenso wie der Multiplikationsfaktor die Kritikalität und damit die Stabilität der Kernspaltungs-Kettenreaktion. Die Reaktivität ρ ist definiert als: und wird meist in Prozent oder auch in Dollar (s. Kritikalität) angegeben. Definitionsgemäß gelten folgende Beziehungen zwischen Reaktivität und Multiplikationsfaktor:
Gegenüber dem Multiplikationsfaktor hat die Reaktivität den Vorteil, näherungsweise additiv zu sein. Werden beispielsweise zwei Absorberstäbe mit Reaktivitätswerten von je 5 Cent in den Reaktorkern eingefahren, verringert sich die Gesamtreaktivität um 10 Cent. Die Explosion des RBMK1000-Reaktors von Tschernobyl im Jahre 1986 beruhte auf einer Reaktivitätsexkursion in den prompt überkritischen Zustand (s. Kritikalität), bei der die Reaktornennleistung Sekundenbruchteile vor der Explosion um mehr als das Hundertfache überschritten wurde. MedizinIn der Physiologie und Pathophysiologie beschreibt die Reaktivität die Fähigkeiten biologischer Gewebe, auf Umwelteinflüsse differenziert zu reagieren (zum Beispiel in der Sinnesphysiologie oder als Immunantwort) und das jeweilige Ausmaß dieser Reaktionen. In der Immunologie ist synonym auch der Begriff der Reagibilität (z. B. als bronchiale Hyperreagibilität beim Asthma bronchiale) gebräuchlich. In der Radiologie und Strahlenbiologie hingegen ist die Reaktivität speziell ein Maß für die Empfindlichkeit von Geweben gegenüber elektromagnetischer Strahlung. [1] Quellen
Kategorien: Chemische Reaktion | Nukleartechnik | Strahlenbiologie |
|
| Dieser Artikel basiert auf dem Artikel Reaktivität aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |