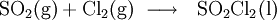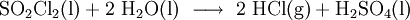Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Sulfurylchlorid
Sulfurylchlorid ist eine farblose, aggressive Flüssigkeit, die zur Gruppe der anorganischen Säurechloride gezählt wird. Es ist das Dichlorid der Schwefelsäure. Produkt-Highlight
Gewinnung und DarstellungEs bildet sich aus Schwefeldioxid und Chlor am Aktivkohlekatalysator: EigenschaftenPhysikalische EigenschaftenSulfurylchlorid ist eine leichtbewegliche, an feuchter Luft rauchende Flüssigkeit, die aufgrund ihres recht niedrigen Siedepunkts von 69 °C leicht verdampft und problemlos durch Destillation gereinigt werden kann. Es hat eine für viele Halogenverbindungen typische hohe Dichte von 1,68 g·cm-3 Chemische EigenschaftenMit Wasser reagiert Sulfurylchlorid unter ausgesprochen heftiger Zersetzung und Wärmeentwicklung zu Schwefelsäure und Chlorwasserstoff: Weiterhin reagiert es heftig mit Basen sowie mit niederen Alkoholen. VerwendungAus Sulfurylchlorid können durch elektrophile aromatische Substitution aromatische Sulfonsäurechloride (Sulfochloride) hergestellt werden. Weiterhin kann es in Gegenwart eines Radikalstarters zur radikalischen Chlorierung von Alkanen und Cycloalkanen verwendet werden. Bei letzterer Reaktion entstehen als gasförmige Nebenprodukte Schwefeldioxid und Chlorwasserstoff. SicherheitshinweiseSulfurylchlorid ist stark ätzend und greift Haut und besonders Schleimhäute und Augen heftig an. Beim Arbeiten ist ein gut ziehender Abzug zu verwenden und die persönlische Schutzausrüstung zu tragen (Kittel, Schutzbrille, Schutzhandschuhe). Reste von Sulfurylchlorid müssen unter größter Vorsicht in kleinen Portionen in eine Eis/Wasser-Mischung eingetragen werden. Die dann erhaltene Schwefelsäure-Salzsäure-Mischung wird mit einer geeigneten Base vorsichtig neutralisiert, bevor sie der fachgerechten Entsorgung zugeführt wird. QuellenKategorien: Ätzender Stoff | Schwefelverbindung | Chlorverbindung | Säurechlorid |
|||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Sulfurylchlorid aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | |||||||||||||||||||||||||||||||||||||||||||||||