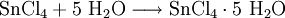Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Zinn(IV)-chlorid
Zinn(IV)-chlorid, manchmal auch einfach Zinnchlorid genannt, ist ein Chlorid des Zinns. Es ist eine klare, rauchende Flüssigkeit, die einen stechenden, salzsäureähnlichen Geruch besitzt. Mit Wasser erfolgt unter starker Erwärmung Hydrolyse zu Zinndioxid. Produkt-Highlight
GeschichteDie erste Erwähnung des Zinnchlorids findet sich 1605 bei Andreas Libavius (daher Spiritus fumans Libavii), aber schon 1630 benutzten es die Holländer in der Cochenillefärberei. HerstellungMan erhält Zinn(IV)-chlorid, indem man Zinn(II)-chlorid-Lösungen von 60 °C mit Salzsäure versetzt und bei 40 °C durch Salpetersäure oxidiert. Die Flüssigkeit erstarrt dann beim Erkalten zu Zinnchlorid mit fünf Molekülen Kristallwasser. Man kann das Zinn(II)-chlorid (Zinnchlorür) auch durch Einleiten von Chlor oxidieren. Zur Darstellung von Zinnchlorid aus Weißblechabfällen, die 3–5 % Zinn enthalten, soll man dieselben mit Chlor behandeln und das verflüchtigte Zinnchlorid in Schlangenröhren verdichten. Die Lösung des Zinnchlorids gibt beim Verdampfen große, zerfließende Kristalle mit fünf Molekülen Kristallwasser. Die verdünnte wässrige Lösung zersetzt sich beim Erhitzen unter Abscheidung von Zinnsäure. Die Dämpfe von Zinnchlorid geben mit Wasserdampf bei Rotglut Zinnsäureanhydrid, mit Schwefelwasserstoff Zinnsulfid. Zinnchlorid dient als Beize in der Färberei und Zeugdruckerei, zur Darstellung von Anilinblau und Farblacken, auch zum Verzinnen. Ammoniumzinnchlorid (NH4)2SnCl6 entsteht beim Vermischen konzentrierter Lösungen von Zinnchlorid und Salmiak als farbloses kristallinisches Pulver, welches sich in drei Teilen Wasser löst, in konzentrierter Lösung Siedetemperatur verträgt, dessen verdünnte Lösung aber beim Erhitzen Zinnhydroxid abscheidet. EigenschaftenZinnchlorid bildet eine farblose Flüssigkeit, raucht an der Luft sehr stark, spez. Gew. 2,234, wirkt höchst ätzend, ist noch bei −20 °C flüssig, siedet bei 120 °C, löst Schwefel, Iod und Phosphor. An der Luft oder wenig Wasser bildet sich das Pentahydrat (Zinnbutter) als kristalline Masse. In größeren Mengen Wasser löst sich das Zinn(IV)-chlorid auf. Lösungen von Zinnchlorid erhält man auch beim Behandeln von Zinnsäure mit Salzsäure, von Zinnchlorürlösung mit Chlor, beim Behandeln einer mit Salzsäure versetzten Zinnchlorürlösung mit Salpetersäure, beim Lösen von Zinn in Königswasser. Letztere Lösung enthält auch Zinn(II)-chlorid (Zinnchlorür) und führt in der Färberei den Namen salpetersaures Zinn, Scharlach-, Zinnkomposition, Zinnsolution, Physik, Rosiersalz, Rosasäure. Statt dieser Lösungen von unsicherem Gehalt kommt jetzt häufiger Zinnchlorid in fester Form in den Handel. VerwendungMan benutzt es unter dem Namen Pinksalz als Beize in der Zeugdruckerei, wo die freie Säure enthaltende Zinnchloridlösung nicht anwendbar ist. Weiterhin dient Zinn(IV)-chlorid zur Herstellung von organischen Zinnverbindungen. Quellen
Kategorien: Ätzender Stoff | Chlorid | Zinnverbindung |
|||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Zinn(IV)-chlorid aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | |||||||||||||||||||||||||||||||||||||||||||||||