Neue Art der Sauerstoffbindung bei Metallen entdeckt – möglicherweise ein „neues Kapitel" der Chemie
Neodym bindet Dioxygen über pi-Wechselwirkungen - ein Novum in der Lanthanidenchemie
Anzeigen
Eisen und Sauerstoff sind im gesamten Körper miteinander verbunden. Am bekanntesten ist die Bindung von Dioxygen, d. h. von zwei miteinander gepaarten Sauerstoffatomen, im Hämoglobin, das den Sauerstoff durch das Blut transportiert. Eisen-Oxo-Verbindungen, wie sie genannt werden, finden sich aber auch an vielen anderen Stellen im Körper. Das hochreaktive Eisen-Oxo wird zum Beispiel in Leberenzymen verwendet, die Medikamente verstoffwechseln.
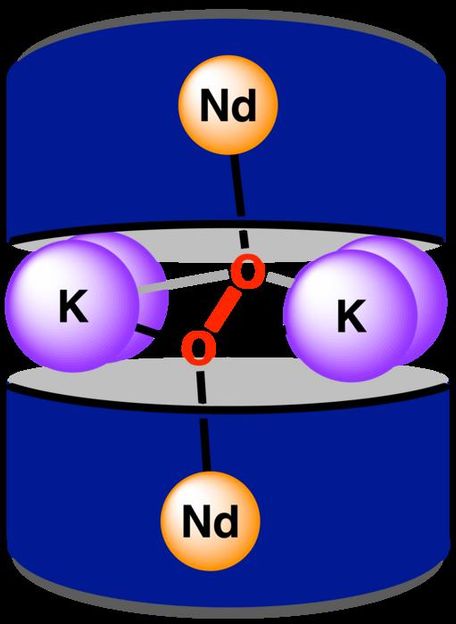
Die oktakoordinierte Ligandenumgebung, die zur Schaffung von pi-Wechselwirkungen zwischen Neodym und Dioxygen verwendet wird
Raúl Hernández Sánchez/Rice University
Der Chemiker Raúl Hernández Sánchez von der Rice University interessierte sich dafür, wie Sauerstoff mit anderen Arten von Metallen reagieren könnte - Metalle, die im untersten Abschnitt des Periodensystems stehen, die so genannten F-Block-Metalle, mit den Lanthaniden in der oberen Reihe und den Actiniden in der unteren. Wenn sich Lanthanoide mit Sauerstoff verbinden könnten, so seine Theorie, würden sie eine hochreaktive Lanthanoid-Oxo-Verbindung bilden, die möglicherweise als synthetischer Ersatz für Eisen-Oxo verwendet werden könnte, was den Chemikern, die an der Erforschung dieser biologischen Reaktionen interessiert sind, einen neuen Werkzeugkasten eröffnen würde.
Das einzige Problem ist, dass f-Block-Metalle, insbesondere Lanthanoide, mit kleinen Molekülen wie Sauerstoff keine pi-Wechselwirkungen eingehen können, eine Art von Wechselwirkung, die für biologische Materialien wie Proteine wesentlich ist. In einer kürzlich im Journal of the American Chemical Society erschienenen Veröffentlichung beschreiben Hernández Sánchez und sein Team einen Weg, um pi-Wechselwirkungen zwischen Dioxygen und einem Lanthanidmetall namens Neodym zu ermöglichen, wodurch Lanthanid-Oxos gebildet werden können.
"Wir hatten eine Ligandenplattform, die wir vor ein paar Jahren entwickelt haben", sagte Hernández Sánchez, Assistenzprofessor für Chemie. "Man kann sich das wie einen Korb vorstellen, der es uns ermöglicht, Metalle einzufangen und sie so zu positionieren, dass bestimmte Bindungen gefördert werden."
Der Korb war gerade groß genug, um ein f-Block-Metallatom aufzunehmen. Das Forschungsteam platzierte zwei Körbe einander gegenüber, wobei sechs sorgfältig platzierte Atome, darunter ein Dioxygenmolekül, die beiden Neodym-Atome miteinander verbanden. So entsteht eine oktakoordinierte Ligandenumgebung, mit der die Positionen der Metalle angepasst werden können.
"Sobald wir das Lanthanid in unserem Ligandenkorb hatten, begannen wir, seine Reaktivität gegenüber kleinen Molekülsubstraten zu erforschen, bis wir die richtigen Bedingungen gefunden hatten, um Dioxygen in einer noch nie dagewesenen Weise zu finden", sagte Hong-Lei Xu, ein Postdoktorand und Erstautor der Arbeit.
Die richtigen Bedingungen ermöglichten, anders als bisher angenommen, Pi-Wechselwirkungen zwischen dem Neodym und dem Sauerstoff, was zu einem Lanthanoid-Oxo-Molekül führte. Chemiker können nun testen, ob diese hochreaktiven Moleküle als synthetischer Ersatz für Eisenoxid verwendet werden können, und wenn ja, welche Möglichkeiten sie bieten, die Eisenoxid nicht hat.
In der Arbeit wurde zwar nur Neodym untersucht, aber das Team von Hernández Sánchez stellt die Hypothese auf, dass eine ähnliche Chemie mit demselben Ligandengerüst auf die meisten Lanthaniden und wahrscheinlich auch Aktiniden ausgedehnt werden kann.
"Die Fähigkeit, Dioxygen an f-Block-Metalle zu binden und die Bindung zwischen den beiden Sauerstoffatomen zu spalten, ermöglicht es uns, potenziell hochreaktive Lanthanid-Oxos freizulegen und Chemikalien mit hohem Mehrwert zu bilden. Wir könnten ein neues Kapitel in der Chemie der Lanthanide aufschlagen", so Hernández Sánchez.
Hinweis: Dieser Artikel wurde mit einem Computersystem ohne menschlichen Eingriff übersetzt. LUMITOS bietet diese automatischen Übersetzungen an, um eine größere Bandbreite an aktuellen Nachrichten zu präsentieren. Da dieser Artikel mit automatischer Übersetzung übersetzt wurde, ist es möglich, dass er Fehler im Vokabular, in der Syntax oder in der Grammatik enthält. Den ursprünglichen Artikel in Englisch finden Sie hier.




































































