Der Katalysator, der nie zur Ruhe kommt
Cu/ZnO/Al₂O₃ wechselt im Betrieb ständig zwischen zwei Strukturzuständen - das könnte der Schlüssel seiner hohen Aktivität sein
Anzeigen
Um seine Funktion genau zu verstehen, untersuchten Forschende der Abteilung Anorganische Chemie des Fritz-Haber-Instituts und des Max-Planck-Instituts für chemische Energiekonversion den Cu/ZnO/Al2O3-Katalysator, der in der Industrie standardmäßig für die Produktion von Methanol eingesetzt wird. Sie fanden heraus, dass die dynamische und temperaturempfindliche Wechselwirkung zwischen Cu und ZnO ein Schlüsselfaktor für die Funktion des Katalysators ist – was neue Impulse für eine gezielte Verbesserung der katalytischen Methanolproduktion gibt.

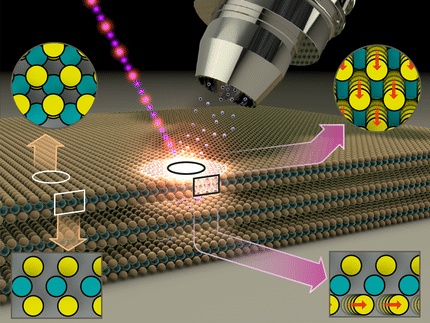
Schematische Darstellung der chemischen und morphologischen Veränderungen, die der Katalysator bei Temperaturänderungen durchläuft. Die Skizze auf der linken Seite zeigt den reversiblen Umwandlungsprozess, der sich aus der mikroskopischen Untersuchung auf der rechten Seite ableitet.
© FHI
Hoffnungsträger Methanol
Methanol (CH3OH) ist aktuell eine der wichtigsten Chemikalien der Welt. Es wird zum Beispiel als Lösungsmittel, bei der Herstellung von Kunststoffen und Farben oder als Treibstoff verwendet. Aufgrund seiner Rolle als Schlüsselprodukt für die chemische Industrie und eine klimaneutrale Energieversorgung ist Methanol von enormer industrieller und ökologischer Bedeutung.
Die Herstellung von Methanol ist ein großtechnischer Prozess, bei dem ein Synthesegas aus Kohlenmonoxid (CO), Kohlendioxid (CO₂) und Wasserstoff (H₂) in einem Reaktor unter Verwendung von Katalysatoren umgewandelt wird. Die Methanolsynthese gilt daher auch als vielversprechender Ansatz für das Recycling von eingefangenem CO₂. Seit den 1960er Jahren werden zur Methanolsynthese in der Industrie Katalysatoren aus Kupfer-Zink-Aluminiumoxid (Cu/ZnO/Al₂O₃) eingesetzt. Es hat sich gezeigt, dass hohe Drücke und moderate Temperaturen die Reaktion begünstigen.
Dennoch ist bislang unklar, wie sich die Katalysatoren unter verschiedenen Reaktionsbedingungen – also „bei der Arbeit“ oder „operando“ – im Detail verhalten und wie sie sich während der Reaktion verändern und entwickeln. Insbesondere sind sich Forschende noch immer nicht im Klaren über die Art und den Ort der synergistischen Effekte zwischen Cu und ZnO und darüber, wo genau sich die aktiven Stellen des Katalysators befinden. Kurz gesagt, ist die Frage: Warum ist genau die Kombination von Cu und ZnO für die Katalyse so gut geeignet?
Der aktuelle Ansatz
Obwohl bekannt ist, dass die hohe Aktivität von Cu/ZnO/Al₂O₃-Katalysatoren auf der Synergie zwischen Cu und ZnO beruht, sind die zugrunde liegenden chemischen Prozesse, einschließlich der Wechselwirkung der Katalysatorkomponenten und der Veränderungen der Katalysatorstruktur unter Reaktionsbedingungen, noch nicht vollständig geklärt.
In dieser Studie wird mithilfe der operando-Transmissionselektronenmikroskopie (TEM) untersucht, wie sich der Cu/ZnO/Al₂O₃-Katalysator „bei der Arbeit“ entwickelt. Die Forschenden betrachten Cu/ZnO/Al₂O₃-Nanopartikel in einem kleinen Reaktor, in dem sie die Reaktionsbedingungen genau anpassen können. Sie beobachten dynamische Strukturveränderungen des Cu/ZnO/Al₂O₃-Katalysators während der Aktivierung und Hydrierung von CO₂ – Schlüsselprozessen bei der Methanolsynthese.
Der “frustrierte” Zustand
Die experimentellen Daten zeigen, dass die Oberfläche des Katalysators hochdynamisch ist. Reversible Strukturveränderungen entstehen in Abhängigkeit von der Temperatur: Beispielsweise öffnen sich ZnOₓ-Schichten auf der Katalysatoroberfläche bei Reaktionstemperaturen über 220 °C, sodass Cu-Oberflächen für die katalytische CO₂-Aktivierung frei werden. Beim Abkühlen bilden sich die ZnOₓ-Schichten wieder, wobei ihre Dicke von der Zusammensetzung des durch den Reaktor strömenden Gases abhängt.
Besonders interessant: die Forschenden formulieren eine Hypothese zu einem ganz besonderen Zustand des Katalysators, einem „frustrierten Phasenübergang“, bei dem der Katalysator ständig und reversibel seine Struktur verändert. Forschende bezeichnen solche Zustände als „frustriert“, da sie niemals zur Ruhe kommen, sondern quasi in einer stetigen Umwandlung zwischen zwei Zuständen „gefangen“ sind, da bestimmte physikalische und chemische Antriebskräfte nicht befriedigt werden können. Im beobachteten frustrierten Zustand wandeln sich während des Betriebs des Katalysators CuZn-Oberflächenbereiche und Cu-ZnO-Grenzflächenstellen auf der Katalysatoroberfläche kontinuierlich ineinander um. Dieses dynamische Gleichgewicht ist wahrscheinlich entscheidend, vielleicht sogar der Schlüssel für die hohe Aktivität und Stabilität des Katalysators.
Schlussfolgerungen
Die Idee hinter der Studie war, die synergistischen Effekte von Cu und ZnO bei der katalytischen CO2-Hydrierung und der Methanolsynthese zu beleuchten. Die Studie beantwortet einige Aspekte dieser Frage: Sie zeigt deutlich, dass die hohe Leistungsfähigkeit von Cu/ZnO/Al₂O₃-Katalysatoren nicht auf einer einzigen aktiven Phase beruht. Vielmehr unterliegt der Katalysator ständigen Strukturveränderungen, wobei seine Aktivität stark von der dynamischen Wechselwirkung zwischen reversibel gebildeten CuZn-Bereichen und Cu-ZnO-Grenzflächen abhängt. Dieser „frustrierte Phasenübergang” ist für die Funktion des Katalysators von zentraler Bedeutung und liefert neue Gestaltungsprinzipien für Katalysatoren der nächsten Generation – für die Methanolsynthese und verwandte Prozesse.
Originalveröffentlichung
Weitere News aus dem Ressort Wissenschaft
Meistgelesene News
Weitere News von unseren anderen Portalen
Verwandte Inhalte finden Sie in den Themenwelten
Themenwelt Synthese
Die chemische Synthese steht im Zentrum der modernen Chemie und ermöglicht die gezielte Herstellung von Molekülen mit spezifischen Eigenschaften. Durch das Zusammenführen von Ausgangsstoffen in definierten Reaktionsbedingungen können Chemiker eine breite Palette von Verbindungen erstellen, von einfachen Molekülen bis hin zu komplexen Wirkstoffen.

Themenwelt Synthese
Die chemische Synthese steht im Zentrum der modernen Chemie und ermöglicht die gezielte Herstellung von Molekülen mit spezifischen Eigenschaften. Durch das Zusammenführen von Ausgangsstoffen in definierten Reaktionsbedingungen können Chemiker eine breite Palette von Verbindungen erstellen, von einfachen Molekülen bis hin zu komplexen Wirkstoffen.