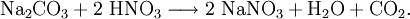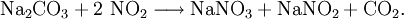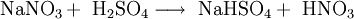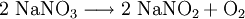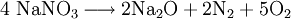Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Natriumnitrat
Natriumnitrat (auch Natronsalpeter oder Chilesalpeter) ist eine chemische Verbindung, das Natriumsalz der Salpetersäure. Im reinen Zustand liegt es in Form einer hygroskopischen (wasseranziehenden), weißen Substanz oder farblosen Kristallen vor. Weiteres empfehlenswertes Fachwissen
VorkommenNatriumnitrat ist das wichtigste natürlich vorkommende Nitrat. Hauptfundort ist Chile, daher auch der Trivialname Chilesalpeter. Weitere natürliche Vorkommen gibt es in Ägypten, Kleinasien, Kolumbien und Kalifornien. GewinnungNatürliche Vorkommen werden durch Filtration von heißen Solen, gewonnen durch Auslaugung mit heißem Wasser, von Fremdstoffen gereinigt. Das in der Kälte auskristallisierte Natriumnitrat hat eine Reinheit von etwa 98 %. Das in den Mutterlaugen enthaltene Iodat geht in die Iodgewinnung. Natriumnitrat kann auch durch Umsatz von Natriumcarbonat mit Salpetersäure gewonnen werden: Hier bietet sich die Absorption von Restgasen der Ammoniakoxidation in konzentrierter Natriumcarbonat-Lösung an: Zur Oxidation des Nitrits wird mit Salpetersäure angesäuert, an der Luft zu Nitrat oxidiert und mit Natriumcarbonat neutralisiert. In Vakuumverdampfern wird es bis zum Feststoff eingeengt. EigenschaftenPhysikalische Eigenschaften
Chemische EigenschaftenIn heißer Schwefelsäure wird es unter Bildung von Salpetersäure zu Natriumhydrogensulfat umgesetzt: Bei Temperaturen oberhalb von 380 °C zersetzt es sich zu Natriumnitrit: Bei Temperaturen oberhalb von 800 °C zu Natriumoxid: Verwendung
LebensmittelzusatzstoffNitrat wirkt gegen Bakterien, vor allem gegen den gefürchteten Botulismus-Erreger (Clostridium botulinum). Beim Pökelprozess wird der chemisch wenig beständige Muskelfarbstoff (Myoglobin) in eine stabilere Variante umgewandelt (Umrötung). Als Folge davon behält das Fleisch seine rote Farbe. Nicht gepökelte Fleisch- und Wurstwaren nehmen eine graue Farbe an, die von den meisten Kunden fälschlicherweise als Hinweis auf einen Verderb angesehen wird. Zudem wird beim Pökeln ein typisches Aroma ausgebildet. Natriumnitrat wird für Wurstwaren, Hartkäse, Schnittkäse, eingelegte Heringe und Sprotten verwendet. Nitrate selbst sind ungefährlich. Problematisch ist ihr Einsatz, weil sie in Nitrite umgewandelt werden. Diese Umwandlung ist im Lebensmittel, aber auch im menschlichen Körper möglich. Nitrite wirken gefäßerweiternd und blutdrucksenkend. In höheren Dosierungen können sie zu akuten Vergiftungserscheinungen führen. (Mangel an Blutfarbstoff Hämoglobin = Blausucht). Nitrit kann mit gleichzeitiger Aufnahme von Protein im menschlichen Körper zu stark krebserregenden Nitrosaminen umgewandelt werden. Nachweis
Quellen
Kategorien: Brandfördernder Stoff | Natriumverbindung | Nitrat |
|||||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Natriumnitrat aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | |||||||||||||||||||||||||||||||||||||||||||||||||