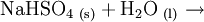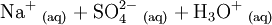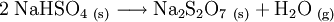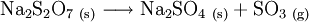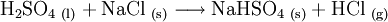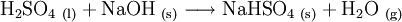Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Natriumhydrogensulfat
Natriumhydrogensulfat (NaHSO4) ist ein saures Natriumsalz der Schwefelsäure. Als Anion enthält es das Hydrogensulfat-Ion. Es wird auch als primäres oder saures Natriumsulfat bezeichnet; ein älterer Name ist Natriumbisulfat. Produkt-HighlightDer weiße, kristalline Feststoff löst sich leicht unter Bildung einer sauren Lösung in Wasser: Erhitzt man das saure Natriumsulfat, so wandelt es sich unter Abgabe von Wasser (Dehydratisierung) in Natriumdisulfat um: Bei weiterem Erhitzen zerfällt das Natriumdisulfat in Natriumsulfat und Schwefeltrioxid: Herstellung
AnwendungenNatriumhydrogensulfat wird zur Senkung des pH-Wertes in Schwimmbecken verwendet, wenn das Wasser zu alkalisch geworden ist. In der Lebensmitteltechnologie dient es als Festigungsmittel, Säureregulator und Trägersubstanz. Natriumhydrogensulfat und Natriumsulfat sind in der EU als Lebensmittelzusatzstoff der Nummer E 514 ohne Höchstmengenbeschränkung (quantum satis) für Lebensmittel allgemein zugelassen.[2] Quellen
Kategorien: Reizender Stoff | Natriumverbindung | Sulfat |
||||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Natriumhydrogensulfat aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | ||||||||||||||||||||||||||||||||||||||||||||||||