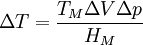Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Schmelzpunkt
Als Schmelztemperatur bezeichnet man die Temperatur, bei der ein Stoff schmilzt, das heißt vom festen in den flüssigen Aggregatzustand übergeht. Die Schmelztemperatur ist abhängig vom Stoff, im Gegensatz zur Siedetemperatur aber nur sehr wenig vom Druck (Schmelzdruck). Schmelztemperatur und Druck werden zusammen als Schmelzpunkt bezeichnet, wobei dieser den Zustand eines Reinstoffes beschreibt und Teil der Schmelzkurve im Phasendiagramm des Stoffes ist. Für reine Stoffe ist der Schmelzpunkt identisch mit dem Gefrierpunkt und bleibt während des gesamten Schmelzvorganges konstant. Durch Verunreinigungen bzw. bei Gemischen wird die Schmelztemperatur in der Regel erniedrigt (Schmelzpunkterniedrigung), außerdem kann die Temperatur während des Schmelzvorganges steigen, wodurch man es mit einem Schmelz-Bereich zu tun hat. Bei amorphen Werkstoffen wie z. B. Gläsern und einigen Kunststoffen spricht man von der Übergangstemperatur. Auch die Bestimmung einer Erweichungstemperatur ist möglich. Manche Stoffe können nicht schmelzen, weil sie vorher chemisch zerfallen, und andere können bei Normalbedingungen nur sublimieren. Die Schmelztemperatur zählt mit der Dichte Risszähigkeit, Festigkeit, Duktilität, Härte, und der Steifigkeit zu den Werkstoffeigenschaften eines Werkstoffes. Weiteres empfehlenswertes Fachwissen
DruckabhängigkeitDer Schmelzpunkt hängt zwar vom Druck ab, allerdings nur geringfügig: Um den Schmelzpunkt um lediglich 1 K zu ändern, muss der Druck durchschnittlich um etwa 100 atm erhöht werden. Daraus folgt, dass sich Änderungen des Atmosphärendrucks – die merkliche Änderungen des Siedepunkts bewirken können – praktisch nicht auf den Schmelzpunkt auswirken. Für das Schmelzen gilt wie für andere Phasenumwandlungen die Clausius-Clapeyronsche Gleichung, die in guter Näherung für das Schmelzen bei verschiedenen Drücken folgende Temperaturänderung ΔT ergibt: Dabei ist TM der Schmelzpunkt, ΔV die Volumenänderung beim Schmelzen, Δp die Differenz der betrachteten Drücke, und HM die Schmelzenthalpie. Da aber die Volumenänderungen ΔV beim Schmelzen relativ klein sind, ist auch die Druckabhängigkeit des Schmelzpunktes relativ klein. Beispielsweise ändert sich bei einer Erhöhung des Drucks um 100 Atm der Schmelzpunkt von Eis um −0,76 K – Eis schmilzt also unter Druck leichter – , während sich der Schmelzpunkt von Tetrachlorkohlenstoff um +3,7 K erhöht. Die Tatsache, dass sich der Schmelzpunkt von Eis oder beispielsweise auch von Bismut bei Druckerhöhung erniedrigt, folgt daraus, dass ihr Volumen beim Schmelzen verringert wird: Dann ist in der obigen Gleichung ΔV und ΔT negativ. BedeutungDer Schmelzpunkt von Wasser hat große Bedeutung in der Biologie und für das Wetter. Die Bestimmung des Schmelzpunkts einer Substanz ist auch von großer Bedeutung in der qualitativen Analytik, einschließlich der Identitätsprüfung, da viele Substanzen über ihren Schmelzpunkt identifiziert werden können. Flüssige Substanzen oder solche mit niedrigem Schmelzpunkt werden dazu in leicht kristallisierende Derivate umgewandelt: Alkohole können beispielsweise durch die Messung der Schmelzpunkte ihrer Ester der Nitrobenzoesäure oder der Dinitrobenzoesäure identifiziert werden. Die Schmelzpunkterniedrigung (Kryoskopie) durch gelöste Substanzen ist der Grund, warum Eis durch Salz geschmolzen werden kann. BestimmungEine ungefähre Messung ist natürlich einfach mit einem Thermometer durch Aufschmelzen der Probe und Ablesen der Schmelztemperatur möglich. Für die exakte Messung des Schmelzpunktes stehen unterschiedliche Methoden zur Verfügung:
Siehe auchPhasendiagramm, molare Schmelzpunkterniedrigung, Siedetemperatur Kategorien: Schwellenwert (Temperatur) | Werkstoffeigenschaft | Stoffeigenschaft |
|||||||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Schmelzpunkt aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |