Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Debye-LängeAls Debye-Länge (nach Peter Debye) bezeichnet man die charakteristische Länge, auf welcher das Potential eines elektrischen Feldes in einem Gemisch von Ladungsträgern unterschiedlicher Polarität auf das Produkt-HighlightDas Prinzip der Abschirmung einer Ladung durch frei bewegliche Ladungsträger entgegengesetzter Polarität ist z.B. anwendbar auf Elektrolyte, Plasmen oder Halbleiter. Debye-Länge in PlasmenIn einem Plasma gilt näherungsweise: λD ist die Debye-Länge, ε0 ist die Elektrische Feldkonstante, kB ist die Boltzmannkonstante, Te ist die Temperatur der Elektronen, ne ist die Elektronendichte, e ist die Elementarladung, also die Ladung eines Elektrons. Obige Formel gilt nur, wenn die Debye-Länge durch die mittlere Energie der Elektronen, also der Elektronentemperatur Te, bestimmt wird. Im allgemeinen Fall gilt: Ti ist die Temperatur der Ionen, Z ist die Ladungszahl der Ionen. Debye-Länge in ElektrolytenIm Elektrolyten gilt:
wobei I die Ionenstärke des Elektrolyten und NA die Avogadro-Konstante ist. Für wässrige Lösungen eines 1:1-Elektrolyten wie etwa Kochsalz ergibt sich bei Raumtemperatur in 0,1-molarer Lösung eine Debyelänge von 0,96 nm, in 0,001 molarer Lösung sind es 9,6 nm. Debye-Länge in HalbleiternFür einen n-Typ Halbleiter gilt: und für einen p-Typ Halbleiter:
Dabei ist εs die Dielektrizitätskonstante des Halbleiters, q die Elementarladung, n0 bzw. p0 die Gleichgewichts-Ladungsträgerdichte des Halbleiters und |
| Dieser Artikel basiert auf dem Artikel Debye-Länge aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |


 -fache abfällt (siehe auch
-fache abfällt (siehe auch 


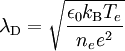
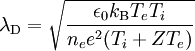
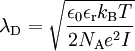 ,
,
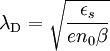
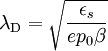 .
.
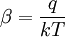 .
.


