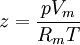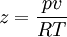Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
KompressibilitätsfaktorDer Kompressibilitätsfaktor (Formelzeichen: z oder Z), auch Kompressions- oder Realgasfaktor, nicht zu verwechseln mit der Kompressibilität, ist ein Begriff der Thermodynamik und dient hier zur Beschreibung der Abweichung eines realen Gases von einem idealen Verhalten. Produkt-HighlightBeschreibungDer Realgasfaktor ist definiert als: oder auch: Hierbei stehen die einzelnen Formelzeichen für folgende Größen:
Nur bei geringem Druck und hohen Temperaturen, sowie bei einem Volumen, das gegen unendlich strebt, verhalten sich reale Gase annähernd ideal, also entsprechend der Zustandsgleichung idealer Gase mit einem Kompressibilitätsfaktor von Eins. Bei höheren Drücken weichen Gase zum Teil erheblich vom idealen Verhalten ab, da sich sowohl Anziehungs- als auch Abstoßungskräfte zwischen den Teilchen bemerkbar machen. Daher ist der Kompressionsfaktor vom Druck und der Temperatur des Gases abhängig (das molare Volumen wiederum ist allein von der Temperatur abhängig). Ein reales Gas ist bei hohem Druck generell schwerer komprimierbar als ein ideales Gas, was einem Kompressibilitätsfaktor größer Eins gleichkommt, wobei jedoch bei einer Drucksteigerung zunächst ein Minimum durchlaufen wird. Am kritischen Punkt des Gases spricht man zudem vom kritischen Kompressibilitätsfaktor oder kritischen Koeffizienten (siehe Van-der-Waals-Gleichung). LiteraturSiehe auch |
| Dieser Artikel basiert auf dem Artikel Kompressibilitätsfaktor aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |