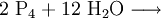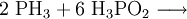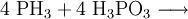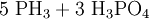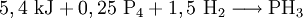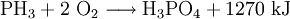Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Monophosphan
Monophosphan, umgangssprachlich etwas unpräzise als Phosphorwasserstoff, Phosphan oder veraltet als Phosphin bezeichnet, gehört zur Gruppe der Phosphane. Monophosphan ist eine chemische Verbindung des Elements Phosphor mit der Summenformel PH3. Es ist ein brennbares, äußerst giftiges, im reinen Zustand geruchloses Gas. Reines Monophosphan ist erst bei 150 °C selbstentzündlich. Durch die Anwesenheit von Diphosphan P2H4 brennt kommerziell erhältliches und im Labor zubereitetes Gas jedoch auch bei Raumtemperatur beim Zutritt von Luft; das Diphosphan und andere Phosphane verleihen diesem gewöhnlichen, nicht ganz reinen Monophosphan einen starken Geruch nach Knoblauch. Produkt-Highlight
Gewinnung und DarstellungEs gibt zahlreiche Möglichkeiten zur Darstellung von Monophosphan. Zum Beispiel disproportioniert weißer Phosphor (P4) im alkalischen Medium zu Phosphan und Phosphinsäure, welche bei höheren Temperaturen zu Monophosphan und Phosphonsäure disproportioniert, welche wiederum zu Phosphorsäure und Monophosphan disproportioniert: Diese Methode wird technisch im Autoklaven bei 250 °C durchgeführt. Analog zur Herstellung von Ammoniak (Haber-Bosch-Verfahren) kann auch eine Synthese aus den Elementen erfolgen: Monophosphan entsteht auch bei der sauren Hydrolyse von salzartigen Phosphiden und Phosphonium-Salzen, sowie bei der Hydridolyse von Phosphorhalogeniden wie z. B. Phosphortrichlorid mit Lithiumaluminiumhydrid in Ether. EigenschaftenPhysikalische EigenschaftenMonophosphan ist in Wasser kaum löslich, die wässrige Lösung reagiert neutral. Das Molekül ist trigonal-pyramidal gebaut. Der Winkel zwischen den einzelnen Wasserstoffatomen beträgt 93,5°. Der Abstand zwischen dem Phosphor– und den Wasserstoffatomen beträgt 1,419 Å.
Chemische EigenschaftenMonophosphan ist eine schwache Base (pKb ~27). Mit Halogenwasserstoffsäuren reagiert es zu unbeständigen Salzen, den sogenannten Phosphoniumsalzen. Bei erhöhter Temperatur zersetzt es sich in die Elementen Wasserstoff und Phosphor. Mit starken Basen wie Natriumamid oder Butyllithium lassen sich die Wasserstoffatome durch Alkalimetalle ersetzen. Durch Substitution sämtlicher Wasserstoffatome lassen sich die sogenannten Phosphide synthetisieren. Das Standard-Reduktionspotential beträgt in im sauren Milieu −0,063 V, im basischen −0,89 V. Deshalb wird Monophosphan bereits bei 150 °C vom Luftsauerstoff zu Phosphorsäure oxidert: VerwendungMonophosphan wird zur Schädlingsbekämpfung, insbesondere zur Mäuse- und Insektenbekämpfung in Getreidesilos und Lagern von Pflanzenprodukten eingesetzt. Die Begasung kann durch Fachkräfte direkt mit Monophosphangas erfolgen. Häufig werden stattdessen feste Präparate (z. B. mit dem Wirkstoff Aluminiumphosphid AlP oder Calciumphosphid Ca3P2) ausgelegt, die mit der Luftfeuchtigkeit reagieren und so das Monophosphangas freisetzen. Es wird auch bei der Herstellung von Leuchtdioden zur Dotierung von Silicium mit Phosphor verwendet. Außerdem wird es zur Synthese diverser organischer Verbindungen verwendet. Es wurden auch schon Versuche zur Phosphordüngung mittels Monophosphan angestellt. PhysiologieMonophosphan ist ein sehr starkes Nerven- und Stoffwechselgift, das nicht nur bei Säugetieren, sondern auch bei Insekten schon bei niedriger Konzentration hochwirksam ist. Beim Menschen löst es Blutdruckabfall, Erbrechen, Lungenödeme und Koma aus. NachweisMonophosphan lässt sich am einfachsten mit sogenannten Drägerröhrchen oder entsprechenden Sensoren nachweisen. Außerdem ist der Geruch von Phosphin (genauer gesagt, der Geruch der enthaltenen Verunreinigungen) ab einer Konzentration von 2 ppm wahrnehmbar. Quellen
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Monophosphan aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||