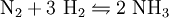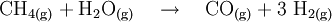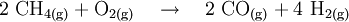Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Haber-Bosch-VerfahrenDas Haber-Bosch-Verfahren ist ein Verfahren zur synthetischen Herstellung von Ammoniak aus den Elementen Stickstoff und Wasserstoff. Es ist benannt nach dessen Entwicklern, den deutschen Chemikern Fritz Haber (1868–1934) und Carl Bosch (1874–1940). Beim Haber-Bosch-Verfahren wird ein Gasgemisch aus Wasserstoff und Stickstoff an einem Eisenoxid-Mischkatalysator aus Eisen(II/III)-Oxid Fe3O4, K2O, CaO, Al2O3 und SiO2 bei etwa 300 bar Druck und 450 °C zur Reaktion gebracht. Aus dem Fe3O4 entsteht im Reaktor durch Reduktion mit H2 der eigentliche Katalysator alpha-Fe. Produkt-Highlight
SynthesebedingungenDie optimalen bzw. ökonomischsten Reaktionsparameter wurden bestimmt auf:
Die Reaktion hat aufgrund der Dreifachbindung des Stickstoffmoleküls trotz Katalysator noch eine hohe Aktivierungsenergie. Diese wird durch die hohe Temperatur aufgebracht. Die Reaktion selbst ist jedoch exotherm (Bildung von 2 NH3: ΔH0= -92,5 kJ/mol); die hohe Temperatur wirkt also der Synthese von Ammoniak entgegen und verringert deshalb die Ausbeute (Prinzip von Le Chatelier). Das Prinzip von Le Chatelier wird jedoch genutzt, indem man das Ammoniak laufend aus dem Reaktionsprozess isoliert, entfernt und durch Frischgas ergänzt und zudem den Druck hoch hält. Der Volumenanteil NH3 im Gasgemisch beträgt rund 17,6 %. Der für die Reaktion nötige Wasserstoff wird heute meist durch die partielle Oxidation von Erdgas erschlossen, der Stickstoff wird wie schon im ursprünglichen Verfahren direkt aus der Luft entnommen. Der störende Sauerstoff wurde früher durch Reduktion mit Wasserstoff zu Wasser umgebildet und dann abgeschieden, heute wird er jedoch bei der Fraktionierung der flüssigen Luft abgetrennt. Moderne Ammoniakanlagen erzeugen bereits mehr als 3.000 Tonnen pro Tag in einer Produktionslinie. Aufgrund der hohen Druck- und Temperaturverhältnisse bei der Synthese des Ammoniaks entfallen etwa 1,1 % des Weltenergieverbrauchs auf das Haber-Bosch-Verfahren. Technische Herstellung von AmmoniakAmmoniak entsteht in einer Gleichgewichtsreaktion aus den Elementen Wasserstoff und Stickstoff. Als erstes werden die Synthesegase benötigt:
In einem ersten Schritt wird Wasserstoff vom Kohlenstoff getrennt. Dazu lässt man Methangas mit Wasserdampf, mit Hilfe eines Katalysators (Nickeloxid-Aluminiumoxid-Katalysator), zu Kohlenstoffmonoxid und Wasserstoff reagieren (Primärreformer).
Da die obige Reaktion das Methangas nur unvollkommen umsetzt, lässt man in einem zweiten Schritt das restliche Methangas mit Sauerstoff zu Kohlenstoffmonoxid und Wasserstoff reagieren (Sekundärreformer). Der Sekundärreformer wird hierzu mit Luft beschickt, wobei der für die spätere Ammoniaksynthese erforderliche Stickstoff automatisch in das Gasgemisch kommt.
In einem letzten Schritt muss das Kohlenstoffmonoxid zu Kohlenstoffdioxid oxidieren (Konvertierung). Kohlenstoffmonoxid und Kohlenstoffdioxid bilden mit Ammoniak Feststoffe (Carbamat), die in kurzer Zeit Rohrleitungen und Apparate verstopfen würden. Im Gegensatz zu Kohlenstoffmonoxid kann Kohlenstoffdioxid durch eine Gaswäsche leicht aus dem Gasgemisch entfernt werden.
Kohlenstoffdioxid wird durch Waschen mit Triethanolamin aus dem Gemisch entfernt. Das oben beschriebene Steamreforming-Verfahren zur Gewinnung von Synthesegas ist das am häufigsten angewendete. Andere mögliche Verfahren sind: 1) Die Partielle Oxidation. Hierbei werden Kohlenwasserstoffe (Von Methangas bis hin zu Steinkohle ist alles möglich) mit Sauerstoff und Wasserdampf in einem offenen Reaktor ohne Katalysator bei ca. 1100°C vergast. Weitere Behandlung des Synthesegases wie beim Steamreformimg. Stickstoff wird vor Eintritt in die Ammoniaksynthese elementar in stöchiometrischer Menge zudosiert. 2) Elektrolyse von Wasser: Hierbei wird mit hohem Aufwand an wertvoller elektrischer Energie Wasser in H2 und O2 zerlegt. Stickstoff wird elementar in stöchiometrischer Menge zudosiert. Dieses Verfahren ist nur wirtschaftlich, wenn billige elektrische Energie z.B. aus Wasserkraft zur Verfügung steht, für die es keine andere Verwendung gibt. 3) Wassergaserzeugung. Hierbei wird der Wasserstoff über die Reaktion von Wasserdampf mit glühendem Koks (siehe Wassergas) hergestellt. Da diese Reaktion endotherm ist, muss man gleichzeitig Luft zuführen. Der Sauerstoff wird der Luft mittels unvollständiger Verbrennung (siehe Generatorgas) entzogen und der für die spätere Ammoniaksynthese erforderliche Stickstoff verbleibt im Wassergas. Anschließend wird das Kohlenstoffmonoxid wie bereits oben beschrieben mittels Konvertierung in leicht zu entfernendes Kohlenstoffdioxid umgewandelt. Dieses Verfahren hat nur noch historische Bedeutung Großtechnische Anwendung
Geschichte und BedeutungDie wesentlichen wissenschaftlichen Leistungen zur Realisierung dieses Verfahrens waren:
Das Haber-Bosch-Verfahren wurde durch die BASF im Jahr 1910 zum Patent angemeldet, ein zuvor eingereichtes fehlerhaftes Patent von Haber zum selben Thema wurde zeitgleich zurückgezogen. Die Weiterentwicklung bis zur großindustriellen Anwendbarkeit fand 1914 auf Druck des deutschen Generalstabsschefs Erich von Falkenhayn statt. Das Deutsche Reich war zu diesem Zeitpunkt durch die britische Seeblockade von den Salpeterlieferungen aus Chile abgeschnitten. Mit Hilfe des Haber-Bosch-Verfahrens gelang es, den schon Ende 1914 drohenden Zusammenbruch der deutschen Munitionsproduktion abzuwenden, und auch eine Düngemittelproduktion aufrecht zu erhalten. Die Explosion des Oppauer Ammoniakwerkes am 21. September 1921 gilt als größte Industriekatastrophe in der deutschen Geschichte. Für die gesamte Entwicklung wurden mehrere Nobelpreise vergeben, z. B. 1918 der Nobelpreis für Chemie an Fritz Haber sowie 1931 für Carl Bosch (zusammen mit Friedrich Bergius), und zwar erstmalig für eine technische Umsetzungsmethode. Das entstandene Ammoniak kann beispielsweise im Ostwaldverfahren zu Salpetersäure oder zu Düngemittel (Reaktion mit CO2 zu Harnstoff) weiterverwendet werden. Salpeter hat eine große Bedeutung für die Rüstungsindustrie, weshalb auch sehr schnell starkes Interesse am Aufbau einer großtechnischen Produktion bestand, die unter anderem in Ludwigshafen-Oppau, Leuna und Bitterfeld durch die BASF und nach Fusion im deutschen Großkonzern der I.G. Farben errichtet und betrieben wurde. Durch den nun in großen Mengen verfügbaren Stickstoffdünger ergab sich Bedarf zu umfangreichen landwirtschaftlichen Forschungen, um nach dem Prinzip der Minimum-Tonne die optimalen Düngermengen je nach Boden und Pflanzenart zu bestimmen. Durch zunehmenden Düngemitteleinsatz konnte die weltweite landwirtschaftliche Produktion deutlich gesteigert werden, was einen weiteren herausragenden, wenn nicht gar den wichtigsten Aspekt der Erfindung des Haber-Bosch-Verfahrens darstellt. Ein weiterer, damals erwünschter Nebeneffekt war die Synthese von kriegstechnisch wertvollem Ammoniumnitrat zur Herstellung von Sprengstoff. Da das Deutsche Reich von natürlichen Stickstoffquellen (v. a. Guano, abgelagerter Vogelkot aus der Region Südpazifik) durch die alliierte Seeblockade während des Ersten Weltkriegs abgeriegelt war, erschloss sich nun eine Möglichkeit, Munition und Sprengstoffe weiterhin höchst effizient herzustellen. Siehe auchLiteratur
|
|
| Dieser Artikel basiert auf dem Artikel Haber-Bosch-Verfahren aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |