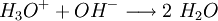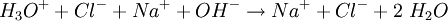Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Neutralisation (Chemie)Unter Neutralisation wird in der Chemie die Aufhebung der (unter anderem) ätzenden Wirkung von Säuren oder Basen (= Laugen) verstanden. Die Grundlage der Neutralisation beruht auf der Tatsache, dass sich die Wirkungen einer Säure und einer Base beim Mischen nicht addieren, sondern aufheben. So kann eine Säure mit einer geeigneten Menge einer Base und eine Base mit einer geeigneten Menge einer Säure neutralisiert werden. Produkt-HighlightIn der Regel finden die Reaktionen in wässrigen Lösungen statt. Starke Säuren bilden in Wasser vollständig H3O + -Ionen, starke Basen OH − -Ionen. Werden solche Lösungen zusammengegeben, bilden sich aus den Hydroxidionen und den Oxoniumionen Wasser. Eine Säure und eine Base sind vollständig neutralisiert, wenn der Neutralpunkt, also der pH-Wert 7 erreicht wird. Die Neutralisation setzt große Energiemengen frei, es handelt sich um eine exotherme Reaktion, es wird Wärmeenergie abgegeben. Beispiel:
Wird eine schwache Säure mit einer starken Base oder eine schwache Base mit einer starken Säure neutralisiert, kann der pH-Wert, bei dem eine vollständige Neutralisation vorliegt, unterschiedlich aufgefasst werden. Der oben genannte pH-Wert 7 entspricht dem Wert von reinem Wasser und kann als "neutral" bezeichnet werden, da die "ätzenden Wirkungen" vollständig aufgehoben sind. Die Komponenten der Säuren und Basen liegen beim Neutralpunkt aber nicht in gleicher Menge vor. In der Chemie wird bei einer vollständigen Neutralisation der pH-Wert beim → Äquivalenzpunkt bevorzugt als neutral bezeichnet. Hier liegen Säuren und Basen in gleicher Menge vor, der pH-Wert weicht aber von 7 ab. |
| Dieser Artikel basiert auf dem Artikel Neutralisation_(Chemie) aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |