Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Osmose
Osmose wird oft, insbesondere in der biologischen Literatur, grob vereinfachend als Phänomen zwischen wässerigen Lösungen beschrieben. Tatsächlich können bei geeigneter Membranbeschaffenheit auch andere Flüssigkeiten sowie Stoffe aus der Gasphase (Gasosmose) durch Osmose übertreten.[1] Von Thermoosmose spricht man, wenn der Stofffluss aufgrund eines Temperaturunterschieds erfolgt.[2] Der Begriff Elektroosmose bezeichnet die Bewegung einer Flüssigkeit an einer elektrochemischen Doppelschicht und wird in einem eigenen Artikel beschrieben. Produkt-Highlight
GeschichtlichesIm Jahre 1784 wurde von Jean-Antoine Nollet ein Experiment beschrieben, bei dem ein mit Weingeist gefüllter und einer entfetteten Schweinsblase verschlossener Zylinder in reines Wasser getaucht wurde. Die Blase blähte sich nach einiger Zeit auf oder zerriss sogar. Das Prinzip der Osmose wurde früh von Henri Dutrochet erforscht, der auch den Namen Osmose prägte. Die erste quantitative Untersuchung des osmotischen Drucks wurde im Jahr 1887 von Wilhelm Pfeffer durchgeführt. Dabei verwendete er die zuvor von Moritz Traube entwickelten Tonzellen als Osmometer (Pfeffersche Zelle).[3] GrundlagenEin Konzentrationsunterschied kann bei der Osmose nur durch Bewegungen des Lösungsmittels (z. B. Wasser) ausgeglichen werden. Das Lösungsmittel auf der Seite mit der geringeren Konzentration wandert durch die Membran auf die Seite der höheren Konzentration. Die Menge des Lösungsmittels auf einer Seite nimmt ab. Auf der anderen Seite wird die Menge des Lösungsmittels erhöht, die Konzentration der gelösten Substanz sinkt. Die Nettobewegung des Lösungsmittels endet, sobald das chemische Potential des Lösungsmittels auf beiden Seiten der Membran gleich ist. In der Abbildung wirkt der hydrostatische Druck der Flüssigkeitsäule dem weiteren Transfer von Lösungsmittel entgegen (siehe Wasserpotential). Tatsächlich findet weiter ein Austausch von Molekülen des Lösungsmittels durch die Membran statt, nur ist im Zustand des Gleichgewichts die Menge der einströmenden Teilchen des Lösungsmittels gleich der Menge der ausströmenden Teilchen. UrsachenAusgeglichene Konzentrationen stellen die thermodynamisch energieärmeren und entropiereichere Zustände dar. Somit führt Osmose zu einer Zunahme an Entropie und einer Abnahme der Energie. Im Falle von Wasser als Lösungsmittel und Ionen als gelöster Substanz gibt es zusätzliche die Erklärung, dass in Wasser gelöste Ionen eine Hydrathülle ausbilden, die zu einer Einschränkung der Bewegungsfreiheit der Wassermoleküle führt. In Folge ist bei höheren Konzentrationsmengen die Bewegung der Wassermoleküle eingeschränkt. Die Wahrscheinlichkeit einer Bewegung der Moleküle auf die Seite mit der geringeren Konzentration ist weniger hoch. Wasserpotential
In biologischen Systemen wie auch in Modellversuchen kann die Bewegung von Wasser durch Membranen nicht allein durch Konzentrationsgefälle der in ihr gelösten Substanzen erklärt werden. Für die Bewegung von Wasser ist vielmehr das Wasserpotenzial entscheidend. Es ist die Summe aus osmotischem Potential und physikalischem Druck. Wird ein U-Rohr in der Mitte durch eine semipermeable Membran geteilt und auf der einen Seite mit destilliertem, auf der anderen mit zuckerhaltigem Wasser gefüllt, wird das Wasser durch die Membran auf die Seite der Zuckerlösung fließen und dort den Spiegel anheben (siehe Abbildung). Die Konzentration gelöster Stoffe kann auf der Seite mit dem destillierten Wasser nicht steigen, dort befinden sich ja gar keine. Würde nur das osmotische Potential allein entscheiden, müsste sämtliches Wasser durch die Membran nach rechts wandern. Durch den erhöhten physikalischen Druck auf der rechten Seite (das Wasser steht höher als links) kommt es jedoch zu einem Ausgleich. Der erhöhte Druck ist so hoch wie die Saugkraft – der negative osmotische Druck – auf der höher konzentrierten Seite. Es ist auch möglich, auf der rechten Seite des U-Rohrs einen Druck anzulegen und so das Wasser aus der bereits konzentrierten Zuckerlösung herauszupressen. Der Prozess wird Umkehrosmose genannt. Auch hier folgt das Wasser dem Wasserpotenzial und nicht nur dem osmotischen Potenzial. Osmose in der BiologieDie Osmose hat eine besondere Bedeutung für biologische Systeme. Hier findet man Zellen, die durch selektivpermeable Membranen voneinander getrennt sind. Diese Membranen sind durch bestimmte Proteine, den Aquaporinen für das Lösungsmittel Wasser durchlässig. Dagegen sind im Wasser gelöste Ionen meistens nicht in der Lage, die Membran zu passieren. Das Wasser in lebenden Zellen ist über die Osmose in die Zellen gelangt. (Weitere Möglichkeit: Pinozytose). Zellen stehen immer im Austausch mit Wasser, z.B. sind Wasserpflanzen oder Algen direkt von Wasser umgeben, auch unsere Zellen werden von Blut und Lymphe umspült. Nehmen wir in einem Experiment die roten Blutkörperchen und überführen sie in ein hypotones Medium wie destilliertes Wasser, werden sie Wasser aufnehmen, bis sie schließlich platzen. Ihre Zellmembranen können nur sehr geringen Drücken standhalten. Viele Pflanzenzellen kann man dagegen in hypotone Lösungen geben, ohne dass sie platzen. Sie besitzen Zellwände, welche einen gewissen Innendruck aushalten. Das Wasser, das von den Pflanzenwurzeln bis in die Blätter transportiert wird, folgt auch den Regeln der Osmose. Das Regenwasser ist hypoton, doch die Wurzelzellen haben ausreichend dicke Zellwände, um einen Turgordruck aufzubauen. Diese Zellen platzen nicht. Einige Viren befreien sich aus infizierten Zellen, indem sie die Zellwand abbauen. Wasser kann nun einströmen, bis die Zellmembran reißt. EnergiefragenAnhand des Experiments mit dem U-Rohr ließe sich ableiten, durch die Osmose würde Energie freigesetzt. Das Konzept wird als Osmosekraftwerk bezeichnet. Dieses würde den Unterschied im Salzgehalt zwischen Süßwasser und Meerwasser nützen, wobei das Salz den gelösten Stoff und das Süßwasser das Lösungsmittel darstellt. Es gibt jedoch noch kein technisches System, das den osmotischen Effekt zur Energiegewinnung nutzt. Berechnung des osmotischen PotentialsIn einem System im thermodynamischen Gleichgewicht bei vorgegebenem Druck und vorgegebener Temperatur ist die Gibbs-Energie minimal und konstant. Es gilt:
Mit den gegebenen Randbedingungen ergibt sich:
Übrig bleiben der Druckterm und der Term des chemischen Potentials. Ist es einer Komponente durch die Membran verwehrt den ganzen Raum auszufüllen, so muss sich der Druck über die Membran ändern um die Gleichung zu erfüllen. Der osmotische Druck π ergibt sich somit mit den molaren Dichten ci aus der Veränderung aller chemischen Potentiale μ zu:
Hierbei sind alle Mischungseffekte berücksichtigt. Da eine derart genaue Berechnung meist mangels Messwerte nicht möglich ist, werden Mischungseffekte der gelösten Salze und die Konzentration des Lösungsmittels manchmal vernachlässigt:
Eine weiter Näherung ist die Vernachlässigung des Mischungseffektes des gelösten Salzes mit dem Lösungsmittel. Hierbei wird die Aktivität ai der gelösten Stoffe gleich 1 gesetzt und es ergibt sich als grobe Näherung:
Diese überschlägige Berechnung kann jedoch leicht einen Fehler von mehr als 50% beinhalten. Wenn die gelösten Stoffe jedoch nur in geringer Konzentration und auf beiden Seiten der Membran in ähnlicher Form vorliegen (wenig Mischungseffekte), ist diese Näherung durchaus üblich. Beispiele
Quellen
Literatur
Siehe auchKategorien: Trennverfahren | Osmose |
|
| Dieser Artikel basiert auf dem Artikel Osmose aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |





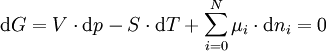
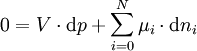 .
.
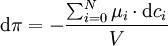 .
.
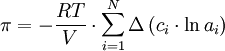 .
.
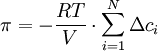 .
.


