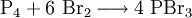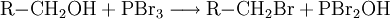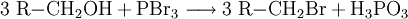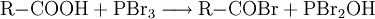Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Phosphortribromid
Phosphortribromid ist eine ätzende chemische Verbindung aus Phosphor und Brom mit der chemischen Formel PBr3. Es gehört zu den Phosphorhalogeniden und liegt als klare, farblose Flüssigkeit vor, die einen charakteristischen, stechenden Geruch hat und an der Luft raucht. Produkt-Highlight
Gewinnung und DarstellungPhosphortribromid lässt sich aus den Elementen darstellen. Dabei wirkt das gebildete Phosphortribromid selbst als Lösemittel für den weißen Phosphor (P4). Um eine Bildung von Phosphorpentabromid (PBr5) zu vermeiden, setzt man Phosphor im Überschuss ein. EigenschaftenPhosphortribromid kann – ähnlich wie Phosphortrifluorid oder Phosphortrichlorid – in Reaktionen – abhängig von den Reaktionspartnern – sowohl als Lewis-Säure als auch als Lewis-Base agieren. Die Geometrie des Phosphortribromidmoleküls ist nicht eben, sondern wie in der Abbildung angedeutet, trigonal-pyramidal (Pyramide mit dreieckiger Grundfläche). Das freie Elektronenpaar am Phosphor beansprucht ebenfalls Raum und verhindert, dass sich die drei Bromatome in einer Ebene mit dem Phosphoratom befinden. Diese Geometrie ähnelt der des Ammoniak-Moleküls. VerwendungPhosphortribromid wird zur Substitution der Hydroxylgruppe primärer und sekundärer – nicht jedoch tertiärer – Alkohole durch Brom eingesetzt[2] . Hierdurch lassen sich Alkylbromide darstellen: Diese Reaktion folgt dem Mechanismus einer SN2-Reaktion. Ein Molekül PBr3 kann bis zu drei Hydroxylgruppen umwandeln. Dabei setzt es sich zu Phosphorsäure um: Analog dazu lassen sich mittels Phosphortribromid aus Carbonsäuren Carbonsäurebromide darstellen: Ferner wird Phosphortribromid bei der α-Bromierung von Carbonsäuren als Katalysator eingesetzt, etwa bei der Hell-Volhard-Zelinsky-Reaktion. In der Mikroelektronik und für Leistungshalbleiter wird PBr3 zur Dotierung von Silizium in Diffusionsöfen verwendet.[3][4] SicherheitshinweisePhosphortribromid und seine Dämpfe sind ätzend. Es reagiert heftig mit Wasser und einer Reihe weiterer Substanzen, wie weißem Phosphor, Alkalimetallen, Alkoholen, Aminen und Ammoniak. Quellen
Kategorien: Ätzender Stoff | Bromverbindung | Phosphorverbindung |
|||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Phosphortribromid aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | |||||||||||||||||||||||||||||||||||||||||||||||