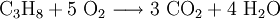Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Propan
Propan ist ein farbloses Gas, es gehört zu den Alkanen, den einfachsten Kohlenwasserstoffen. Produkt-Highlight
EigenschaftenPropan ist ein farb- und geruchloses Gas, hat einen Schmelzpunkt von −187,7 °C und einen Siedepunkt von −42 °C. Der kritische Punkt liegt bei 94 °C (369,82 K = 96,67 °C laut „Handbook of Chemistry and Physics“ 76th Edition, 1995–1996) und 4,24 MPa. Propan kann also leicht verflüssigt werden. Es löst sich sehr gering bei 20 °C zu 80 mg/l in Wasser. Es ist hochentzündlich, schwerer als Luft und wirkt in hohen Konzentrationen narkotisierend bis erstickend. Propan ist hochentzündlich und bildet zwischen einem Volumenanteil von 1,7 % bis 10,8 % in Luft explosive Gemische. Seine Zündtemperatur liegt bei 470 °C (nach DIN 51794). Der Heizwert beträgt 12,874kWh/kg (Butan 12,700kWh/kg). Verwendung und HerstellungPropan wird aus Erdgas gewonnen oder in einer Erdölraffinerie beim Cracken von Erdöl hergestellt. Es dient verflüssigt als Brenn- und Heizgas (Flüssiggas), etwa bei Pkw als Autogas oder für den Heißluftballon, sowie als Kältemittel (Kältemittelbezeichnung R290) (siehe Kühlschrank), als möglicher Bestandteil des Treibmittels in Sprays und Softairs (meist wird jedoch, aufgrund des geringeren Drucks, Butan eingesetzt) sowie zur Herstellung von Ethylen und Propen. LagerungPropan wird unter Druck verflüssigt in Gasflaschen oder Tanks gelagert. Weiterhin wird es auch in unterirdischen Kavernen gelagert. Das Einlagern geschieht vorzugsweise in den verbrauchsarmen Monaten, um Verbrauchsspitzen im Winter abdecken zu können. ReaktionenPropan verbrennt zu Kohlendioxid und Wasser. Literatur
Kategorien: Feuergefährlicher Stoff | Alkan | Gas |
|||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Propan aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | |||||||||||||||||||||||||||||||||||||||||||||||