Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Pyrit
Pyrit ist ein Mineral mit der chemischen Formel FeS2 und gehört zur Mineralklasse der Sulfide. Das Anion ist allerdings kein normales Sulfid-Ion, sondern ein Disulfid-Ion S22−, das strukturell dem Peroxid-Ion entspricht. Synonym für Pyrit ist Schwefelkies, der chemische Name ist Eisen(II)-disulfid. Es kristallisiert im kubischen Kristallsystem und hat eine Härte von 6 bis 6,5. Idiomorphe Kristalle, das sind Kristalle mit vollständiger Ausbildung der Eigengestalt, haben meist die Form von Würfeln oder Pentagondodekaedern. Auch Oktaeder und Disdodekaeder sind verbreitet, sowie Kombinationen zwischen diesen Formen. Pyrit ist polymorph zu Markasit. Sein metallischer Glanz und seine goldene Farbe brachten dem Pyrit den Beinamen Katzengold ein, der sich von dem Wort „Ketzer“ ableitet. Eine weitere, seltenere Bezeichnung ist Narrengold, ein wahrscheinlich inkorrekter Anglizismus (fool's gold). Anders als echtes Gold ist Pyrit aber nicht formbar und wesentlich härter als das Edelmetall. Allerdings enthält Pyrit kleine Mengen Gold, die es zu einem wirtschaftlich abbaubaren Golderz machen können. Pyrit ist ein natürlicher Halbleiter, dessen Energielücke zwischen Valenzband und Leitungsband durch Einbau von Fremdatomen herabgesetzt ist. Eine Dotierung mit Arsen führt zu einem p-Halbleiter [2] Die Bandlücke liegt zwischen 0,8 und 1,8 eV. Ob es sich dabei um direkte oder indirekte Bandkantenübergänge handelt ist noch unklar. Für den indirekten Übergang wird meist eine Energie von 0,95 eV angegeben.[1] Die Dielektrizitätskonstante Produkt-Highlight
VorkommenPyrit ist bei Weitem das meistverbreitete Sulfidmineral, er ist Bestandteil der meisten Sulfidlagerstätten und Beimineral der meisten mafischen Gesteine. Auch in Hydrothermaladern, wo es durch Kristallisierung eisensulfidhaltiger Lösungen entstehen kann, findet es sich. Die Weichteile von Tieren werden in stagnierenden sauerstofffreien schlammigen Milieus oft durch Pyrit ersetzt, so dass Pyrit auch in Sedimentgesteinen auftritt. Schwefelreduzierende Bakterien sind hier für die Ablagerung kleinster Kristalle verantwortlich, die sich dann bei Verdichtung der Ablagerungen zu Gestein wandeln. Bei stärkerer Komprimierung kann Pyrit zu größeren Kristallen wachsen und sogar Muschelschalen oder Knochen ersetzen. Auf diese Weise können Fossilien komplett umgewandelt werden. Ein Beispiel hierfür sind die als Goldschnecken bezeichneten Ammoniten des Jura der Fränkischen Alb. Unter Sauerstoffeinfluss an der Erdoberfläche verwittert Pyrit über mehrere Zwischenstufen zu Eisenoxidhydrat (Limonit oder Brauneisenerz) FeO.OH. Schließlich kommt Pyrit auch in Braun- und Steinkohle sowie in sauerstofffreien Grundwasserleitern vor. Es ist in dieser Umgebung meist schlecht kristallisiert und sehr oxidationsempfindlich - die beiden nachstehenden Bilder geben davon einen Eindruck. Im zweiten der genannten Bilder ist framboidaler Pyrit zu erkennen; der Name leitet sich von dem französischen Wort framboise für „Himbeere“ ab und spielt auf die kugelige Gestalt des Pyritüberzugs an. Weltweit gibt es viele Vorkommen von großen Pyritmassen („Kieskörper“). Gut kristallisierten Pyrit gibt es u.a. auf der Insel Elba und in Peru. Berühmtheit besitzen die Pyrit-Zwillingskristalle („Eisernes Kreuz“) aus dem Weserbergland der Umgebung von Vlotho und im Extertal. Bedeutung als RohstoffWirtschaftlich wird Pyrit zur Gewinnung von Schwefelsäure abgebaut, gelegentlich auch zur Goldgewinnung. Der bei der Schwefelsäuregewinnung übrigbleibende Rückstand, das Purpurerz (Fe2O3) wird in Hochöfen zu Eisen verarbeitet. Bei Kupferanteilen über 0,5 Prozent wird auch Kupfer gewonnen. Bis 1992 lag eine der wichtigsten großbetrieblich ausgebeuteten Vorkommen in Deutschland bei Meggen im Sauerland. Bedeutung für die UmweltDer in Braunkohle und Steinkohle enthaltene Pyrit und andere Schwefelverbindungen geben im Verbrennungsprozess den enthaltenen Schwefel als Schwefeldioxid (SO2) an die Rauchgase ab. Wenn dieses Gas in die Atmosphäre gelangt, bildet sich in Wassertröpfchen schweflige Säure, die wesentlich zum Entstehen des „sauren Regens“ beiträgt. Durch Maßnahmen der Rauchgasentschwefelung kann das Schwefeldioxid heute weitgehend zurückgehalten werden. Auch der in grundwasserführenden Schichten enthaltene Pyrit kann in Gegenwart von Sauerstoff oxidiert werden. Diese Oxydation ist weit überwiegend durch Bakterien katalysiert. Eine große Bedeutung hat die Oxidation des Pyrits durch denitrifizierende, eisen- und schwefeloxidierende Bakterien mit Nitrat als mittelbares Oxidationsmittel. Dies ist ein aus mehreren abiotischen und bakteriellen Redoxreaktionen bestehender Prozess, bei dem letztendlich der Sulfidschwefel des Pyrits zu Sulfat (SO42-) oxidiert wird und Nitrat zu elementarem, molekularem Stickstoff (N2) reduziert wird. Man bezeichnet diesen Vorgang als „Denitrifikation“ durch Pyrit. In den Wassergewinnungsgebieten der Stadtwerke Hannover AG werden auf diese Weise jährlich größenordnungsmäßig 1000 Tonnen Pyrit umgesetzt. Da nach der Trinkwasserverordnung der Grenzwert für Nitrat mit 50 mg/l niedriger ist als der für Sulfat mit 240 mg/l, bedeutet die Denitrifikation durch Pyrit im Hinblick auf die Einhaltung des Nitratgrenzwertes eine Entlastung. Das im Pyrit enthaltene Eisen und andere metallische Begleitelemente wie Mangan oder Nickel können teilweise in das Wasser übertreten und müssen bei der Trinkwasseraufbereitung eliminiert werden. Pyrit und FeuersteinDer Name Pyrit stammt aus dem griechischen πυρ pyr für Feuer. Mit einem harten Feuerstein lassen sich Pyrit-Splitter abschlagen, die sich entzünden und verbrennen:
EsoterikDer Pyrit soll - laut vielen esoterischen Richtungen - das Selbstbewusstsein steigern und von Ängsten befreien. Wissenschaftlich ist dies jedoch nicht belegt. GalerieSiehe auchEinzelnachweise
Kategorien: Schmuckstein | Mineral | Eisenmineral | Sulfide und Sulfosalze | Kubisches Kristallsystem | Schwefelmineral |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Pyrit aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||


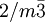
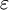 von Pyrit beträgt 20,8.
von Pyrit beträgt 20,8.


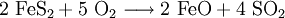 Diese Eigenschaft wurde früher genutzt um Zunder zu entzünden und Feuer zu machen.
Diese Eigenschaft wurde früher genutzt um Zunder zu entzünden und Feuer zu machen.


