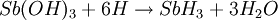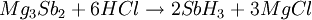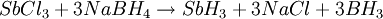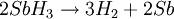Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Stiban
Stiban (Monostiban oder Antimonwasserstoff, veraltet auch als Stibin bezeichnet), chemische Formel SbH3, ist ein farbloses, übelriechendes und äußerst giftiges Gas, das bei der Auflösung von salzartigen Antimoniden in Wasser und verdünnten Säuren entsteht. Produkt-Highlight
Gewinnung und DarstellungStiban wird aus löslichen Antimonverbindungen und naszierendem Wasserstoff gewonnen. So entsteht bei der Reaktion von Antimon(III)-hydroxid mit naszierendem Wasserstoff Stiban und Wasser.
Eine andere Möglichkeit besteht darin, Magnesiumantimonid in einem Überschuss verdünnter Salzsäure zu lösen.
Beide Methoden bringen jedoch den Nachteil mit sich, dass das entstehende Gas hauptsächlich aus Wasserstoff besteht. Durch abkühlen des Gases auf unter −17 °C kann dieser jedoch abgetrennt werden, da Stiban bei dieser Temperatur kondensiert. Eine Methode, die diesen Nachteil nicht mit sich bringt, ist die Hydrierung von Antimon(III)-chlorid mittels Natriumborhydrid in salzsaurer Lösung.
EigenschaftenPhysikalische EigenschaftenDer Schmelzpunkt liegt bei −88 °C, der Siedepunkt bei −17 °C. Die Gibbs-Energie ΔfG0g beträgt 148 kJ/mol, die Standardentropie S0g 233 J/(mol·K) und die Wärmekapazität Cp0g 41 J/(mol·K).[3] Stiban ist ein pyramidales Molekül mit den drei Wasserstoff-Atomen an der dreieckigen Pyramidenbasis und dem Antimon-Atom an der Pyramidenspitze. Die Winkel H-Sb-H betragen 91.7°, der Abstand Sb-H beträgt 1.707 Å. Chemische EigenschaftenDie chemischen Eigenschaften des Stibans ähneln dem Arsenwasserstoff. Typisch für ein Schwermetallhydrid ist Stiban instabiler als die jeweiligen Elemente. Bei Raumtemperatur zerfällt das Gas langsam, bei 200 °C jedoch sehr schnell. Dieser Prozess verläuft autokatalytisch und unter Umständen explosiv.
Mit starken Brønsted-Basen lässt sich Stiban unter Bildung von Antimoniden deprotonieren. VerwendungStiban wird in der Halbleiterindustrie zur n-Dotierung von Silicium verwendet. SicherheitshinweiseAufgrund der hohen Toxizität und der leichten Entflammbarkeit ist beim Umgang mit Stiban Vorsicht geboten. Es sollte mit Schutzkleidung und Schutzmaske, fernab von offenen Flammen und Funkenbildung gehandhabt werden. Einatmen von Stiban kann zu Husten, Übelkeit, Hals- und Kopfschmerzen, Mattigkeit, blutigem Urin und zu Atemnot führen. Es können Schädigungen des Blutes, der Leber, der Nieren und des Zentralnervensystems auftreten, die zum Tod führen können. Aufgrund der Instabilität sollte Stiban wenn möglich nicht gelagert werden. NachweisStiban lässt sich mit der Marsh'schen Probe nachweisen. Hierzu wird Stiban, vermischt mit Wasserstoff, durch ein dünnes, zu einer Spitze ausgezogenem Glasrohr, geleitet und am Ende abgefackelt. Dabei wird das Glasrohr mit einem Bunsenbrenner erhitzt, wobei sich Anwesenheit von Stiban im Glasrohr ein Antimonspiegel bildet. Der Antimonspiegel unterscheidet sich von einem Arsenspiegel durch seine dunklere Farbe, außerdem ist er in Natriumhypochloritlösung unlöslich. Literatur
Quellen
Kategorien: Giftiger Stoff | Feuergefährlicher Stoff | Antimonverbindung | Wasserstoffverbindung |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Stiban aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||