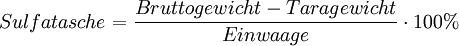Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
SulfatascheSulfatasche bezeichnet sowohl ein chemisch-analytisches Verfahren als auch dessen Produkt (Substanz) und Ergebnis (Wert). Produkt-HighlightSulfatasche ist ein gravimetrisches Verfahren, das zur Bestimmung anorganischer Bestandteile in einer organischen Probe dient. Es unterscheidet sich dadurch von anderen Veraschungen, dass vor dem Glühen Schwefelsäure zugesetzt wird. Dadurch werden evtl. vorhandene Alkalihalogenide in schwerer flüchtige Alkalisulfate umgewandelt. Dies soll verhindern, dass es neben der erwünschten Verflüchtigung der organischen Bestandteile (vgl. Asche) auch Alkalihalogenide in die Gasphase übergehen und damit nicht mehr erfasst werden. Da die zugrunde liegenden chemischen Vorgänge komplex und uneinheitlich sind, muss bei der Analyse nach einem genau festgelegten Verfahren vorgegangen werden (Konventionsmethode). Das Europäische Arzneibuch schreibt z.B. folgende Vorgehensweise vor: 1. Porzellan- oder Platintiegel 30 min. zur Rotglut erhitzen 2. Erkaltenlassen im Exsikkator und wiegen (Taragewicht) 3. Vorgeschriebene Menge der Substanz (Einwaage) mit 10%iger Schwefelsäure (2 ml) versetzen 4. Tiegel zunächst im Wasserbad, dann über offener Flamme, dann bis 600 °C glühen bis alle schwarzen Teile entfernt sind 5. Tiegel erkalten lassen und erneut 10%ige Schwefelsäure (einige Tropfen) zugeben 6. Erhitzen und Glühen (siehe 4.) 7. Glühen (je 15 min) – Erkalten – Wiegen (bis zur Massenkonstanz, Bruttogewicht) Der prozentuale Anteil des im Tiegel verbliebenen Rückstands wird als Sulfatasche bezeichnet und mit der (Reinheits-)Anforderung der jeweiligen Arzneibuch-Monografie verglichen.
|
| Dieser Artikel basiert auf dem Artikel Sulfatasche aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |