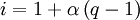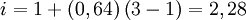Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Van 't Hoff-FaktorIn der Physikalischen Chemie bezeichnet der Van 't Hoff-Faktor i das Verhältnis der Stoffmenge eines Soluts in einer wässrigen Lösung zur Stoffmenge des ursprünglich zugegebenen festen Ausgangsstoffs. Der Faktor ist damit ein Maß für die Löslichkeit, also dafür, wie gut bzw. vollständig sich ein Stoff in Wasser löst und insbesondere dafür, wie viele Teilchen sich danach in Lösung befinden. Die Bezeichnung geht auf Jacobus Henricus van 't Hoff zurück, den ersten Träger des Nobelpreises für Chemie. Produkt-HighlightBerechnungDie Berechnung des Van't Hoff-Faktors erfolgt über folgende Gleichung:
BeispieleAls Beispiel hat Glukose einen Van't Hoff-Faktor von 1, denn sie ist vollständig in Wasser lösbar. Demgegenüber ist der Van't Hoff-Faktor von Natriumchlorid gleich 2, denn ein Mol NaCl dissoziiert in je ein Mol Na+ und Cl-. Stoffe wie schwache Elektrolyte, die nur teilweise dissoziieren, haben folglich einen gebrochenen Van't Hoff-Faktor je nach dem jeweiligen Dissoziationsgleichgewicht. Für Schwefelsäure (H2SO4) zeigt sich so beispielsweise ein Van't Hoff-Faktor von 2,28, da 64 % der Schwefelsäuremoleküle in je ein Sulfat- und zwei Wasserstoff- bzw. Hydroniumionen dissoziiert. BedeutungDer Van't Hoff-Faktor spielt vor allem bei kolligativen Prozesse eine wichtige Rolle, da es hier auf die absolute Teilchenzahl und nicht die Art der Teilchen ankommt. |
| Dieser Artikel basiert auf dem Artikel Van_'t_Hoff-Faktor aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |