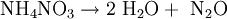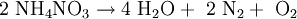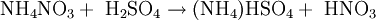| Strukturformel
|
|
|
| Allgemeines
|
| Name
| Ammoniumnitrat
|
| Andere Namen
|
- Ammonsalpeter
- Ammonialsalpeter
- brennbarer Salpeter
- salpetersaures Ammonium
- Ammonnitrat
- Ammonium nitricum
|
| Summenformel | NH4NO3
|
| CAS-Nummer | 6484-52-2
|
| Kurzbeschreibung | weißer, pulvriger Feststoff
|
| Eigenschaften
|
| Molare Masse | 80,04 g·mol−1
|
| Aggregatzustand | fest
|
| Dichte | 1,725 g·cm−3 (20 °C)[1]
|
| Schmelzpunkt | 169,6 °C[1]
|
| Siedepunkt | 210 °C (15 mbar), bei Normaldruck Zersetzung ab 170 °C[1]
|
| Dampfdruck
|
nicht anwendbar[2]
|
| Löslichkeit
|
bei 20 °C 1177 g/l in Wasser, löslich in Methanol
|
| Sicherheitshinweise
|
| Gefahrstoffkennzeichnung
[1]
|
| R- und S-Sätze
| R: 8-9}}}">{{{3}}}}}}">{{{4}}}}}}">{{{5}}}}}}">{{{6}}}}}}">{{{7}}}}}}">{{{8}}}}}}">{{{9}}}}}}">{{{10}}}}}}">{{{11}}}}}}">{{{12}}}}}}">{{{13}}}}}}">{{{14}}}
}}
}}
}}
}}
}}
}}
}}
}}
}}
}}
}}
}}
}}
|
}}
}}[1]
|
| S: 15-16-41}}}">{{{4}}}}}}">{{{5}}}}}}">{{{6}}}}}}">{{{7}}}}}}">{{{8}}}}}}">{{{9}}}}}}">{{{10}}}
}}
}}
}}
}}
}}
}}
}}
}}
}}
|
}}
}}
}}[1]
|
|
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen.
|
Ammoniumnitrat ist das Salz, das sich aus Ammoniak und Salpetersäure bildet.
Herstellung
Ammoniumnitrat (NH4NO3) entsteht durch Neutralisation von Ammoniak mit Salpetersäure.
Verwendung
Ammoniumnitrat ist der Hauptbestandteil vieler Düngemittel (Blaukorn, Kalkammonsalpeter) und gewerblicher Sprengstoffe, beispielsweise des Sprengmittels ANFO.
Eigenschaften
Beim Erhitzen (T < 300 °C) zerfällt Ammoniumnitrat gemäß der Gleichung
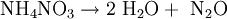
in Wasser und Lachgas. Durch starke Initialzündung beziehungsweise Erhitzen über 300 °C zerfällt es folgendermaßen:
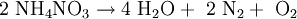
Das Nitrat-Ion NO3− (Oxidationsstufe von N: +V) oxidiert dabei das Ammonium-Ion NH4+, (Oxidationsstufe −III). Im Produkt, N2, sind beide Stickstoffatome auf gleicher Oxidationsstufe (0). Eine solche Reaktion, bei der ein Atom ein anderes Atom des selben Elements oxidiert heißt Komproportionierung.
Der explosionsartige Übergang vom Feststoff (NH4NO3) zu den gasförmigen Produkten Stickstoff, Sauerstoff und Wasserdampf erklärt die hohe Sprengkraft.
Durch Reaktion mit konzentrierter Schwefelsäure und anschließender Destillation lässt sich die Salpetersäure zurückgewinnen, welche die Ausgangssubstanz zur Herstellung vieler Explosivstoffe ist:
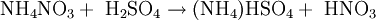
Die Chemikalie gilt als brandfördernd und kann beim Erhitzen explodieren. In der Bundesrepublik Deutschland ist der Umgang mit den durchsichtigen und farblosen Kristallen durch das Sprengstoffgesetz geregelt. In Düngemitteln darf Ammoniumnitrat wegen seiner latenten Gefahr nur in Mischungen verwendet werden.
Bei Zugabe von Ethanol in Ammoniumnitrat in wässriger Lösung fällt es aus.
Katastrophen
- Eine große Katastrophe war die Explosion des Oppauer Ammoniakwerkes am 21. September 1921. Dort wurde routinemäßig vor dem Versand ein festgewordenes Dünger-Gemisch aus Ammoniumnitrat und Ammoniumsulfat mit Dynamit gelockert. Vermutlich aufgrund eines Fehlers beim Mischungsverhältnis kam es bei einer solchen Explosion zu einer Initialzündung, die dann insgesamt 4500 Tonnen des Gemisches zur Explosion brachte und einen der größten Explosionsschäden der Geschichte verursachte: 561 Menschen kamen ums Leben und ein großer Teil der Fabrik und der umliegenden Bebauung waren zerstört.
- Am 16. April 1947 explodierten im Hafen von Texas City (Texas, USA) die mit Ammoniumnitrat beladenen Frachter Grandcamp (Frankreich) und Highflyer (USA). Es gab 486 Tote, über 100 Vermisste, 3000 Verletzte, Hunderte Obdachlose und 65 Millionen US-Dollar Schaden. [1]
- Am 28. Juli 1947 explodierte im Hafen von Brest (Frankreich) der mit Ammoniumnitrat beladene Frachter Ocean Liberty (Norwegen): 21 Tote, über 100 Verletzte und 2 Millionen Pfund Schaden.
- Bei dem Bombenanschlag auf das Murrah Federal Building in Oklahoma City (USA) am 19. April 1995 verwendete der Attentäter Timothy McVeigh eine Mischung aus Ammoniumnitrat und einem Brennstoff (Nitromethan). Bei dem Anschlag wurde ein neunstöckiges Bürogebäude durch eine Autobombe zerstört, 168 Menschen kamen ums Leben.
- Am 21. September 2001 - exakt 80 Jahre nach der Katastrophe von Oppau - starben bei einer Ammoniumnitrat-Explosion in Toulouse 31 Menschen.
- Am 22. April 2004 ereignete sich im nordkoreanischen Ryongchŏn eine verheerende Explosion eines mit Ammoniumnitrat beladenen Zugwaggons. 154 Menschen starben, nach Schätzungen wurden ca. 1200 Menschen verletzt und ca. 8000 Häuser zerstört oder beschädigt. Siehe Zugunglück von Ryongchŏn
Siehe auch
Quellen
- ↑ a b c d e f Eintrag zu Ammoniumnitrat in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 3.9.2007 (JavaScript erforderlich)
- ↑ Sicherheitsdatenblatt (Merck)
Literatur
- Richard Escales: Ammonsalpetersprengstoffe. Survival Press, 1909, Reprint 2002, ISBN 3831135630
- K. Hahnefeld, R. Gill, G. Buske: Einflussgrößen auf Detonationsfähigkeit von Ammoniumnitrat. Wirtschaftsverlag NW, Bremerhaven 1983, ISBN 3883143081
Wiki/Weblinks
- http://www.wortlastig.de/text/oppau.htm
- http://k23.hydra.xnode.at/knitrat.htm
- http://chembel.de/Firmen/Bergchemie/vfeuerwasser.htm
- http://www.seilnacht.com/Chemie/ch_ammn.htm
- http://zeus.zeit.de/text/archiv/2001/41/200141_toulouse.xml
|