Die Säure in der Nano-Pore
Wasser in Zeolithen hilft bei der Umwandlung von Biomasse in Biosprit
Anzeigen
Zeolithe sind extrem poröse Materialien: Zehn Gramm davon können eine innere Oberfläche von der Größe eines Fußballfeldes besitzen. Ihre Hohlräume lassen sich nutzen, um chemische Reaktionen zu katalysieren und damit Energie zu sparen. Ein internationales Forschungsteam hat nun neue Erkenntnisse über die Rolle von Wassermolekülen in diesen Prozessen gewonnen. Eine wichtige Anwendung ist die Umwandlung von Biomasse in Biosprit.
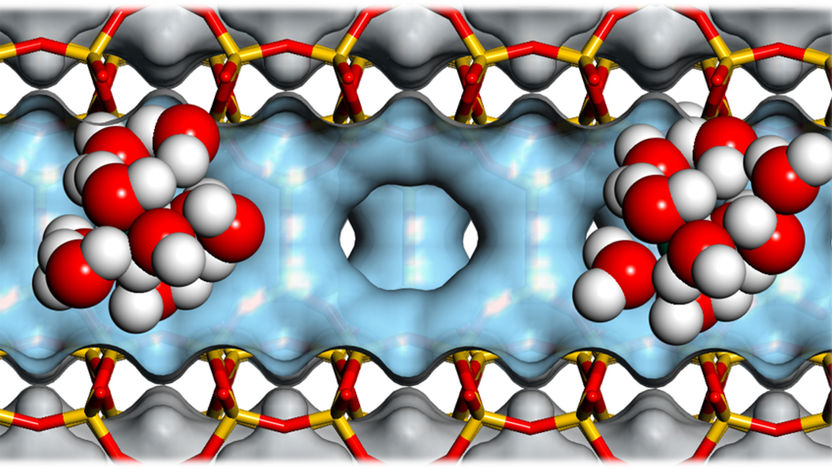
Wassercluster in den Poren eines Zeoliths
Andreas Jentys / TUM
Treibstoff aus Biomasse gilt zwar als klimaneutral, dennoch benötigt man Energie um ihn herzustellen: Erst höhere Temperaturen und Druck sorgen dafür, dass die gewünschten chemischen Reaktionen stattfinden.
„Wenn wir in Zukunft auf fossile Energieträger verzichten und Biomasse im großen Stil effizient nutzen wollen, dann müssen wir auch Wege finden, den Energiebedarf bei der Verarbeitung zu reduzieren“, sagt Johannes Lercher, Professor für Technische Chemie an der Technischen Universität München (TUM) und Direktor am Institute for Integrated Catalysis am Pacific Northwest National Laboratory in Richland, Washington (USA).
Zusammen mit einem internationalen Forschungsteam hat der Chemiker sich jetzt die Rolle von Wassermolekülen bei Reaktionen innerhalb der nur wenige Nanometer großen Poren in Zeolithen genauer angesehen.
Das Saure an der Säure
Eine Säure zeichnet sich dadurch aus, dass sie bereitwillig Protonen abgibt. Salzsäure spaltet sich so auf in ein negativ geladenes Chlorid-Anion, wie es auch im Kochsalzkristall vorkommt, und ein positiv geladenes Proton, das in Wasser an Wassermoleküle andockt. Es entsteht so ein positiv geladenes Hydronium-Ion, das dieses Proton aber auch gerne wieder weiter reicht, beispielsweise an ein organisches Molekül.
Wird diesem ein Proton „aufgedrängt“, versucht es sich zu stabilisieren. Aus einem Alkohol kann so ein Molekül mit einer Doppelbindung werden – ein typischer Reaktionsschritt auf dem Weg von Biomasse zu Biosprit. Die Wände von Zeolithen stabilisieren die bei der Umwandlung auftretenden Übergangszustände und helfen so, den Energieaufwand für die Reaktion zu minimieren.
Ein Zeolith wird sauer
In Zeolithen gibt es Sauerstoffatome im Kristallverband, die bereits ein Proton besitzen. Im Zusammenspiel mit Wassermolekülen bilden sie, wie molekulare Säuren, Hydronium-Ionen.
Während die sich im Wasser jedoch verteilen, sind sie im Zeolithen fest gebunden. Durch chemische Vorbehandlung kann man die Zahl dieser aktiven Stellen variieren und so in den Poren des Zeolithen eine bestimmte Dichte von Hydronium-Ionen herstellen.
Der optimale Zeolith für jede Reaktion
Das Forschungsteam variierte nun systematisch die Größe der Hohlräume, die Dichte der aktiven Zentren und die Wassermenge. So konnte es zeigen, welche Porengröße und welche Wassermenge ausgewählte Beispielreaktion am besten katalysiert.
„Grundsätzlich kann man die Reaktionsgeschwindigkeit steigern, indem man die Poren enger macht und die Ladungsdichte erhöht“, erklärt Johannes Lercher. „Diese Steigerung hat allerdings Grenzen: Wenn es zu eng wird und die Ladungen zu dicht nebeneinander sind, nimmt die Reaktionsgeschwindigkeit wieder ab. Für jede Reaktion kann man so die optimalen Bedingungen finden.“
„Zeolithe sind für alle chemischen Reaktionen geeignet, deren Reaktionspartner in diese Poren hineinpassen und bei denen eine Säure als Katalysator eingesetzt wird“, betont Lercher. „Wir stehen hier ganz am Anfang einer Entwicklung die das Potenzial hat, die Reaktivität von Molekülen auch bei niedrigen Temperaturen deutlich zu erhöhen und damit bei der Gewinnung von Kraftstoffen oder chemischen Substanzen in erheblichem Umfang Energie einzusparen.“
Originalveröffentlichung
Niklas Pfriem, Peter H. Hintermeier, Sebastian Eckstein, Sungmin Kim, Qiang Liu, Hui Shi, Lara Milakovic, Yuanshuai Liu, Gary L. Haller, Eszter Baráth, Yue Liu, Johannes A. Lercher; "Role of the ionic environment in enhancing the activity of reacting molecules in zeolite pores"; Science; May 28, 2021: Vol. 372, Issue 6545, pp. 952-957





































































