Gefunden: Der "Heilige Gral der Katalyse"
Umwandlung von Methan in Methanol unter Umgebungsbedingungen mit Hilfe von Licht
Anzeigen
Ein internationales Forscherteam unter der Leitung von Wissenschaftlern der Universität Manchester hat eine schnelle und wirtschaftliche Methode zur Umwandlung von Methan oder Erdgas in flüssiges Methanol bei Umgebungstemperatur und -druck entwickelt. Das Verfahren findet unter kontinuierlichem Fluss über ein photokatalytisches Material statt, das sichtbares Licht als Antrieb für die Umwandlung nutzt.
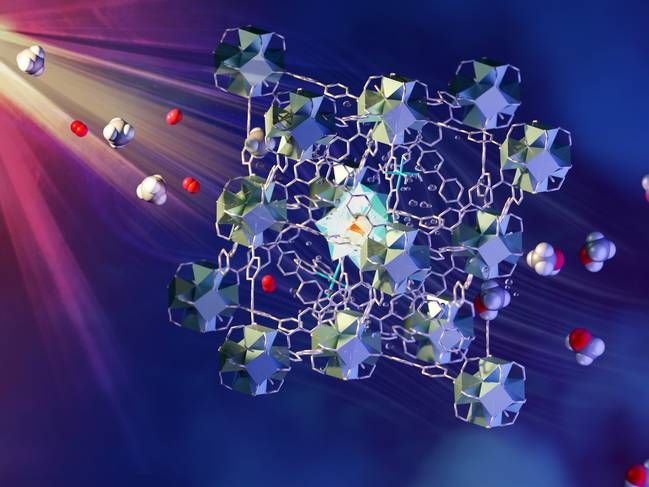
Ein internationales Forscherteam unter der Leitung von Wissenschaftlern der Universität Manchester hat eine schnelle und wirtschaftliche Methode zur Umwandlung von Methan oder Erdgas in flüssiges Methanol bei Umgebungstemperatur und -druck entwickelt. Das Verfahren findet unter kontinuierlichem Fluss über ein photokatalytisches Material statt, das sichtbares Licht zur Umwandlung nutzt.
ORNL/Jill Hemman
Um zu beobachten, wie der Prozess funktioniert und wie selektiv er ist, nutzten die Forscher die Neutronenstreuung am VISION-Instrument an der Spallationsneutronenquelle des Oak Ridge National Laboratory.
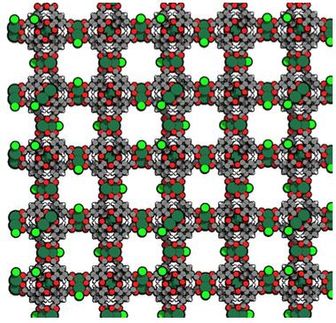
Die Methode beinhaltet einen kontinuierlichen Fluss von mit Methan/Sauerstoff gesättigtem Wasser über einen neuartigen metallorganischen Gerüstkatalysator (MOF). Das MOF ist porös und enthält verschiedene Komponenten, die jeweils eine Rolle bei der Absorption von Licht, der Übertragung von Elektronen und der Aktivierung und Zusammenführung von Methan und Sauerstoff spielen. Das flüssige Methanol lässt sich leicht aus dem Wasser extrahieren. Ein solches Verfahren wird gemeinhin als "heiliger Gral der Katalyse" bezeichnet und ist ein Schwerpunkt der vom US-Energieministerium unterstützten Forschung. Einzelheiten zu den Ergebnissen des Teams mit dem Titel "Direct photo-oxidation of methane to methanol over a mono-iron hydroxyl site" sind in Nature Materials veröffentlicht .
Natürlich vorkommendes Methan ist ein reichlich vorhandener und wertvoller Brennstoff, der für Öfen, Wassererhitzer, Brennöfen, Automobile und Turbinen verwendet wird. Methan kann jedoch auch gefährlich sein, da es schwierig zu fördern, zu transportieren und zu lagern ist.
Methangas ist auch umweltschädlich, wenn es freigesetzt wird oder in die Atmosphäre entweicht, wo es ein starkes Treibhausgas ist. Zu den wichtigsten Quellen für atmosphärisches Methan gehören die Produktion und Nutzung fossiler Brennstoffe, verrottende oder verbrennende Biomasse wie Waldbrände, landwirtschaftliche Abfallprodukte, Mülldeponien und auftauender Permafrost.
Überschüssiges Methan wird in der Regel verbrannt oder abgefackelt, um seine Umweltauswirkungen zu verringern. Bei diesem Verbrennungsprozess entsteht jedoch Kohlendioxid, das selbst ein Treibhausgas ist.
Die Industrie ist seit langem auf der Suche nach einer wirtschaftlichen und effizienten Möglichkeit, Methan in Methanol umzuwandeln, einen äußerst marktgängigen und vielseitigen Rohstoff, der zur Herstellung einer Vielzahl von Konsum- und Industrieprodukten verwendet wird. Dies würde nicht nur dazu beitragen, die Methanemissionen zu verringern, sondern auch einen wirtschaftlichen Anreiz dafür bieten.
Methanol ist eine vielseitigere Kohlenstoffquelle als Methan und eine leicht zu transportierende Flüssigkeit. Es kann zur Herstellung von Tausenden von Produkten wie Lösungsmitteln, Frostschutzmitteln und Acrylkunststoffen, synthetischen Stoffen und Fasern, Klebstoffen, Farben und Sperrholz sowie chemischen Wirkstoffen für Arzneimittel und Agrarchemikalien verwendet werden. Auch die Umwandlung von Methan in einen hochwertigen Kraftstoff wie Methanol wird angesichts der schwindenden Erdölreserven immer attraktiver.
Die Bindung brechen
Eine der größten Herausforderungen bei der Umwandlung von Methan (CH4) in Methanol (CH3OH) ist die Schwierigkeit, die chemische Kohlenstoff-Wasserstoff-Bindung (C-H) zu schwächen oder zu brechen, um ein Sauerstoffatom (O) zur Bildung einer C-OH-Bindung einzufügen. Herkömmliche Methanumwandlungsverfahren umfassen in der Regel zwei Stufen, die Dampfreformierung und die anschließende Syngasoxidation, die energieintensiv, kostspielig und ineffizient sind, da sie hohe Temperaturen und Drücke erfordern.
Das von dem Forscherteam entwickelte schnelle und wirtschaftliche Verfahren zur Umwandlung von Methan in Methanol nutzt ein Mehrkomponenten-MOF-Material und sichtbares Licht, um die Umwandlung voranzutreiben. Ein mit CH4 undO2 gesättigter Wasserstrom wird durch eine Schicht des MOF-Granulats geleitet, während es dem Licht ausgesetzt wird. Das MOF enthält verschiedene Komponenten, die an festen Positionen innerhalb der porösen Struktur angeordnet sind. Sie arbeiten zusammen, um Licht zu absorbieren und Elektronen zu erzeugen, die an Sauerstoff und Methan in den Poren abgegeben werden, um Methanol zu bilden.
"Wenn Methangas dem funktionellen MOF-Material mit Mono-Eisen-Hydroxyl-Stellen ausgesetzt wird, fördern die aktivierten Sauerstoffmoleküle und die Energie des Lichts die Aktivierung der C-H-Bindung im Methan, um Methanol zu bilden", so Sihai Yang, Chemieprofessor in Manchester und korrespondierender Autor. "Der Prozess ist zu 100 % selektiv - d. h. es entsteht kein unerwünschtes Nebenprodukt - vergleichbar mit der Methan-Monooxygenase, die in der Natur das Enzym für diesen Prozess ist."
Die Experimente haben gezeigt, dass der feste Katalysator isoliert, gewaschen, getrocknet und für mindestens 10 Zyklen oder etwa 200 Stunden Reaktionszeit wiederverwendet werden kann, ohne dass es zu einem Leistungsverlust kommt.
Der neue photokatalytische Prozess ist analog dazu, wie Pflanzen während der Photosynthese Lichtenergie in chemische Energie umwandeln. Pflanzen nehmen über ihre Blätter Sonnenlicht und Kohlendioxid auf. Ein photokatalytischer Prozess wandelt diese Elemente dann in Zucker, Sauerstoff und Wasserdampf um.
"Dieser Prozess wurde als der 'heilige Gral der Katalyse' bezeichnet. Anstatt Methan zu verbrennen, könnte es nun möglich sein, das Gas direkt in Methanol umzuwandeln, eine hochwertige Chemikalie, die zur Herstellung von Biokraftstoffen, Lösungsmitteln, Pestiziden und Kraftstoffzusätzen für Fahrzeuge verwendet werden kann", so Martin Schröder, Vizepräsident und Dekan der Fakultät für Wissenschaft und Technik in Manchester und korrespondierender Autor. "Dieses neue MOF-Material könnte auch in der Lage sein, andere Arten von chemischen Reaktionen zu erleichtern, indem es als eine Art Reagenzglas dient, in dem wir verschiedene Substanzen kombinieren können, um zu sehen, wie sie reagieren."
Mit Neutronen zum Bild des Prozesses
"Der Einsatz von Neutronenstreuung zur Aufnahme von 'Bildern' mit dem VISION-Instrument bestätigte zunächst die starken Wechselwirkungen zwischen CH4 und den Mono-Eisen-Hydroxyl-Stellen im MOF, die die C-H-Bindungen schwächen", so Yongqiang Cheng, Instrumentenwissenschaftler im ORNL Neutron Sciences Directorate.
"VISION ist ein Neutronenschwingungsspektrometer mit hohem Durchsatz, das optimiert wurde, um Informationen über die molekulare Struktur, chemische Bindungen und intermolekulare Wechselwirkungen zu liefern", so Anibal "Timmy" Ramirez Cuesta, Leiter der Gruppe Chemische Spektroskopie bei SNS. "Methanmoleküle erzeugen durch ihre Rotation und Vibration starke und charakteristische Neutronenstreuungssignale, die auch auf die lokale Umgebung reagieren. Dies ermöglicht es uns, die bindungsschwächenden Wechselwirkungen zwischen CH4 und dem MOF mit fortschrittlichen Neutronenspektroskopietechniken eindeutig aufzudecken."
Schnell, wirtschaftlich und wiederverwendbar
Da keine hohen Temperaturen oder Drücke erforderlich sind und die Energie des Sonnenlichts zum Antrieb des Photooxidationsprozesses genutzt wird, könnte die neue Umwandlungsmethode die Kosten für Ausrüstung und Betrieb erheblich senken. Die höhere Geschwindigkeit des Prozesses und seine Fähigkeit, Methan ohne unerwünschte Nebenprodukte in Methanol umzuwandeln, werden die Entwicklung einer Inline-Verarbeitung erleichtern, die die Kosten minimiert.
Hinweis: Dieser Artikel wurde mit einem Computersystem ohne menschlichen Eingriff übersetzt. LUMITOS bietet diese automatischen Übersetzungen an, um eine größere Bandbreite an aktuellen Nachrichten zu präsentieren. Da dieser Artikel mit automatischer Übersetzung übersetzt wurde, ist es möglich, dass er Fehler im Vokabular, in der Syntax oder in der Grammatik enthält. Den ursprünglichen Artikel in Englisch finden Sie hier.