Die Kraft des Goldes freisetzen: ein Durchbruch in der grünen Chemie
Forscher haben eine starke Synergie zwischen Gold, Mangan und Kupfer entdeckt, die die Art und Weise, wie wir wertvolle Chemikalien herstellen, verändern könnte
Anzeigen
Acetaldehyd ist ein wichtiges chemisches Zwischenprodukt, das traditionell über das Ethylen-basierte Wacker-Oxidationsverfahren hergestellt wird, das sowohl kostspielig als auch umweltschädlich ist. Die selektive Oxidation von Bioethanol zu Acetaldehyd bietet eine umweltfreundlichere und nachhaltigere Alternative, doch die meisten bekannten Katalysatoren kämpfen mit dem üblichen Kompromiss zwischen Aktivität und Selektivität und liefern in der Regel weniger als 90 % Acetaldehyd.
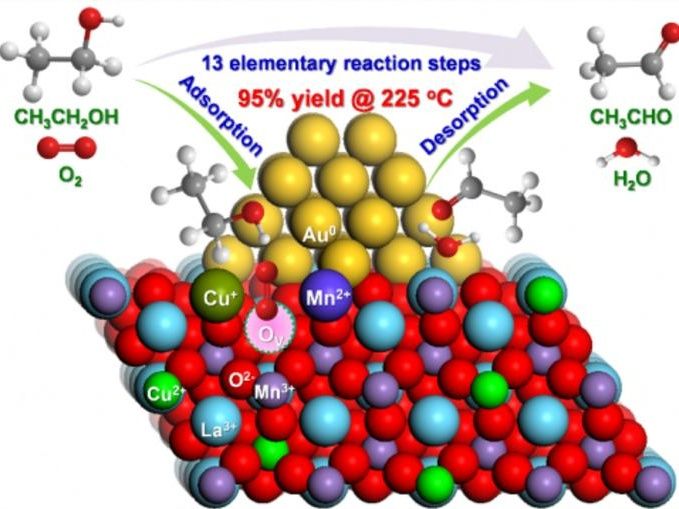
Forscher haben eine starke Synergie zwischen Gold, Mangan und Kupfer entdeckt, die die Art und Weise, wie wir wertvolle Chemikalien herstellen, verändern könnte. Durch das Aufbringen winziger Goldnanopartikel auf ein speziell entwickeltes Perowskit-Material (LaMn0,75Cu0,25O3) erzielte das Team eine beeindruckende Ausbeute von 95 % an Acetaldehyd aus Ethanol bei nur 225 °C - ein wichtiger Schritt in Richtung sauberer, effizienterer chemischer Prozesse. Das Geheimnis liegt in der intelligenten Verwendung von Kupfer. Eine kleine Menge Kupfer verbessert den Katalysator dramatisch, indem es aktive Stellen schafft, die den schwierigsten Schritt der Reaktion beschleunigen. Doch die Sache hat einen Haken: Zu viel Kupfer destabilisiert das System und verringert die Effizienz. Dieses empfindliche Gleichgewicht unterstreicht die Bedeutung des Designs auf atomarer Ebene bei Katalysatoren der nächsten Generation für eine nachhaltige chemische Produktion.
Chinese Journal of Catalysis
Liu und Hensen wiesen eine spezifische Au0-Cu+-Synergie im modernen Au/MgCuCr2O4-Katalysator nach und erzielten eine AC-Ausbeute von über 95 % bei 250°C mit einer stabilen Leistung von über 500 Stunden (J. Am. Chem. Soc. 2013, 135, 14032; J. Catal. 2015, 331, 138; J. Catal. 2017, 347, 45). Trotz dieses bedeutenden Schritts, der vor mehr als einem Jahrzehnt gemacht wurde, bleibt die Suche nach effizienteren, ungiftigen Katalysatoren, die die selektive Ethanoloxidation bei niedrigeren Temperaturen fördern können, eine große Herausforderung.
Kürzlich meldete das Forscherteam unter der Leitung von Prof. Peng Liu (Huazhong University of Science and Technology) und Prof. Emiel J.M. Hensen (Eindhoven University of Technology) bedeutende Fortschritte bei der selektiven Ethanoloxidation. Sie entwickelten eine Reihe von Au/LaMnCuO3-Katalysatoren mit unterschiedlichen Mn/Cu-Verhältnissen, von denen die Au/LaMn0,75Cu0,25O3-Zusammensetzung einen ausgeprägten Synergieeffekt zwischen Goldnanopartikeln und mäßig Cu-dotiertem LaMnO3-Perowskit aufwies. Diese Synergie ermöglichte eine effiziente Oxidation von Ethanol bei Temperaturen unter 250°C und übertraf damit den zuvor getesteten Au/MgCuCr2O4-Katalysator. Die Ergebnisse wurden im Chinese Journal of Catalysis veröffentlicht.
Um die Effizienz der Umwandlung von Bioethanol in Acetaldehyd - eine wertvolle Chemikalie, die in Kunststoffen und Arzneimitteln verwendet wird - zu verbessern, entwickelten die Forscher eine neue Klasse von Katalysatoren auf der Grundlage von Perowskit-Materialien. Diese Träger wurden durch eine Sol-Gel-Verbrennungsmethode synthetisiert und anschließend mit Goldnanopartikeln beschichtet. Durch Anpassung des Verhältnisses von Mangan zu Kupfer in der Perowskit-Struktur ermittelte das Team eine optimale Zusammensetzung (Au/LaMn0,75Cu0,25O3), mit der eine hohe Acetaldehydausbeute von 95 % bei 225 °C erzielt wurde und die Leistung 80 Stunden lang stabil blieb. Katalysatoren mit höherem Kupfergehalt waren weniger effektiv, vor allem weil Kupfer dazu neigt, seine aktive Form während der Reaktion zu verlieren. Die verbesserte Leistung des optimierten Katalysators ist auf eine kooperative Wechselwirkung zwischen Gold-, Mangan- und Kupferionen zurückzuführen.
Um besser zu verstehen, wie diese Elemente zusammenwirken, setzten die Forscher fortschrittliche Berechnungsmethoden ein, darunter Dichtefunktionaltheorie und mikrokinetische Simulationen. Diese Studien ergaben, dass durch die Dotierung des Perowskits mit Kupfer aktive Stellen in der Nähe der Goldpartikel entstehen, die eine effizientere Aktivierung von Sauerstoff- und Ethanolmolekülen ermöglichen. Der optimierte Katalysator wies auch eine niedrigere Energiebarriere für wichtige Reaktionsschritte auf, wodurch der Prozess effizienter wurde. Sowohl die experimentellen als auch die theoretischen Ergebnisse zeigen, wie wichtig die Feinabstimmung der Katalysatorzusammensetzung ist, um eine bessere Leistung zu erzielen.
Hinweis: Dieser Artikel wurde mit einem Computersystem ohne menschlichen Eingriff übersetzt. LUMITOS bietet diese automatischen Übersetzungen an, um eine größere Bandbreite an aktuellen Nachrichten zu präsentieren. Da dieser Artikel mit automatischer Übersetzung übersetzt wurde, ist es möglich, dass er Fehler im Vokabular, in der Syntax oder in der Grammatik enthält. Den ursprünglichen Artikel in Englisch finden Sie hier.