Neue Katalysator-Strategie ersetzt energieintensives Haber-Bosch-Verfahren
Elektrochemische Nitratreduktion mit Kupferoxid produziert Düngemittel-Grundstoff ohne hohe Temperaturen
Anzeigen
Forscher der Tokyo Metropolitan University haben herausgefunden, wie ein Katalysator in einer für die Industrie vielversprechenden chemischen Reaktion zur Herstellung von Ammoniak, einem wichtigen Bestandteil von Düngemitteln, beiträgt. Kupferoxid ist ein Schlüsselkatalysator in der elektrochemischen Nitratreduktionsreaktion, einer umweltfreundlicheren Alternative zum bestehenden Haber-Bosch-Verfahren. Sie entdeckten, dass Kupferpartikel mitten in der Reaktion entstehen und dabei helfen, Nitrit-Ionen in Ammoniak umzuwandeln. Dieser Einblick in die zugrundeliegenden Mechanismen verspricht einen großen Fortschritt bei der Entwicklung neuer industrieller Chemie.
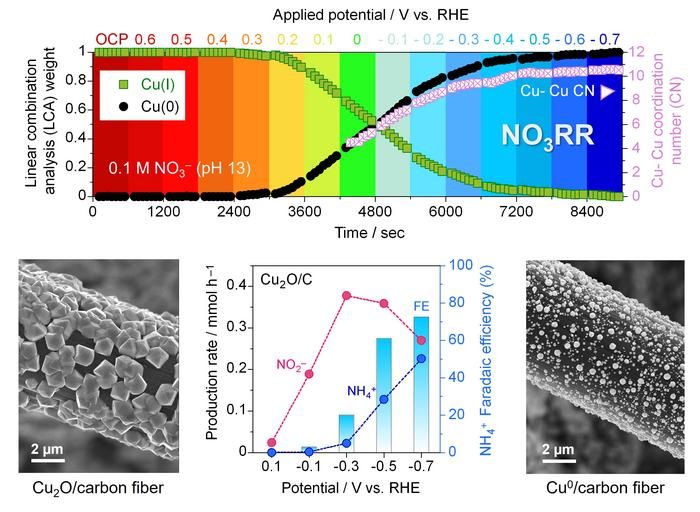
(oben) Anteil von Kupfer (I) in Kupferoxid und Kupfer (0) in metallischen Kupferpartikeln bei verschiedenen angelegten Spannungen. Eine negativere Spannung korreliert mit dem Auftreten von mehr Cu-Cu-Bindungen. (unten links) Rasterelektronenmikroskopische (REM) Aufnahme von Kupferoxidpartikeln, die auf Kohlenstofffasern aufgebracht sind. (unten Mitte) Produktionsrate von Nitrit- und Ammonium-Ionen bei verschiedenen Spannungen und Effizienz der Ammonium-Produktion. (unten rechts) REM-Aufnahme von metallischen Kupferpartikeln auf Kohlenstofffasern.
Tokyo Metropolitan University
Als Bestandteil von Düngemitteln ist Ammoniak eine wichtige Chemikalie in der industriellen Landwirtschaft. Die am weitesten verbreitete Methode zur Herstellung von Ammoniak ist das Haber-Bosch-Verfahren, bei dem Stickstoff und Wasserstoff bei hoher Temperatur und hohem Druck umgesetzt werden. Dies macht das Verfahren energieintensiv; es soll für etwa 1,4 % der weltweiten Kohlendioxidemissionen verantwortlich sein. Da es sich um eine Chemikalie handelt, die für einen Großteil der Lebensmittelproduktion benötigt wird, wird nach umweltfreundlicheren Wegen zur Herstellung von Ammoniak gesucht.
Ein Team unter der Leitung von Professor Fumiaki Amano von der Tokyo Metropolitan University hat die elektrochemische Nitratreduktionsreaktion untersucht, eine vielversprechende Alternative, mit der Ammoniak bei Raumtemperatur und Druck aus Nitraten hergestellt werden kann. Bei elektrochemischen Prozessen werden Elektroden in ein chemisches Gemisch eingebracht und eine Spannung angelegt, um Reaktionen auszulösen. Trotz zahlreicher Studien, in denen spezifische Reaktionen an den Elektroden bei der Herstellung von Ammoniak identifiziert wurden, konnte der genaue Mechanismus bisher nicht aufgeklärt werden.
Mit Hilfe modernster Techniken gewann das Team einen beispiellosen Einblick in die Art und Weise, wie Ammoniak in Gegenwart eines Kupferoxid-Katalysators, einem der effektivsten Elektrokatalysatoren für diese Art von Reaktion, erzeugt wird. Sie verwendeten Operando-Röntgenabsorption, eine Methode, die Einblicke in elektronische Zustände mit Kenntnissen über lokale Bindungen und Strukturen kombiniert. Indem sie kleine Kupferoxidpartikel auf Kohlenstofffasern montierten, konnten sie herausfinden, wie sich die Zustände ändern, wenn die Spannung während der Reaktion negativ wird. Bei positiver Spannung zeigte sich, dass die Nitrat-Ionen den Katalysator "passivieren", indem sie an ihm absorbiert werden und die Umwandlung von Kupferoxid in metallisches Kupfer verhindern, wobei stattdessen Nitrit-Ionen entstehen. Wenn die Spannung negativer wird, steigt die Ammoniakproduktion abrupt an. Dies geschieht zur gleichen Zeit wie das Auftreten metallischer Kupferpartikel, was sich in einer drastischen Zunahme der Anzahl von Kupfer-Kupfer-Bindungen zeigt. Sie entdeckten, dass das metallische Kupfer dazu beiträgt, den Nitrit-Ionen Wasserstoff hinzuzufügen, um Ammoniak zu erzeugen.
Die Messungen des Teams haben gezeigt, wie sich die Oberflächenpassivierung auf die Effizienz des Kupferoxid-Katalysators auswirkt und wie entscheidend die Produktion von metallischem Kupfer für die effiziente Herstellung von Ammoniak ist. Ihre Arbeit zeigt eine breite Klasse von Strategien zur Optimierung der grünen Ammoniakproduktion und zur Entwicklung neuer elektrochemischer Katalysatoren auf.
Diese Arbeit wurde von der Tokyo Metropolitan University und dem Tokyo Global Partner Scholarship Program unterstützt und basiert auf Ergebnissen des Projekts JPNP14004, das von der New Energy and Industrial Technology Development Organization (NEDO) in Auftrag gegeben wurde.
Hinweis: Dieser Artikel wurde mit einem Computersystem ohne menschlichen Eingriff übersetzt. LUMITOS bietet diese automatischen Übersetzungen an, um eine größere Bandbreite an aktuellen Nachrichten zu präsentieren. Da dieser Artikel mit automatischer Übersetzung übersetzt wurde, ist es möglich, dass er Fehler im Vokabular, in der Syntax oder in der Grammatik enthält. Den ursprünglichen Artikel in Englisch finden Sie hier.


































































