Vom Gestank zum Wertstoff
Gewinnung von Schwefel und Wasserstoff: Spaltung von Schwefelwasserstoff durch Solarenergie
Anzeigen
Keiner, der schon mal ein faules Ei aufgeschlagen hat, wird wohl den infernalischen Gestank vergessen. In Biogasanlagen, Klärwerken und Erdölraffinerien können sogar ganz erhebliche Mengen des widerlich riechenden, in höheren Konzentrationen giftigen Schwefelwasserstoffgases entstehen. Ein australisch-chinesisches Forscherteam stellt in der Zeitschrift Angewandte Chemie einen innovativen photoelektrochemischen Ansatz vor, mit dem sich das unerwünschte Nebenprodukt unter Nutzung von Sonnenenergie in Schwefel und Wasserstoff spalten und so als Rohstoffquelle nutzen lässt.
Mit mehreren Techniken wird Schwefelwasserstoff (H2S) aus belasteter Abluft entfernt und bisher nur vereinzelt genutzt. Während Schwefel in einigen Verfahren rückgewonnen werden kann, gelingt dies mit dem enthaltenen Wasserstoff noch nicht. Schade eigentlich, denn gerade Wasserstoff ist ein wichtiger Energielieferant für die zukunftsträchtige Brennstoffzellentechnik.
Leider kann man H2S aber nicht einfach spalten und im selben Verfahren Schwefel und Wasserstoff gewinnen. Besonders attraktiv erscheint die photochemische Spaltung, denn dabei kann Sonnenenergie den hohen Energiebedarf der Reaktion decken. Bisher ließ sich allerdings noch kein ökologisch und ökonomisch sinnvoller Prozess realisieren. Dies könnte sich dank eines neuen Ansatzes ändern, der vom Team um Lianzhou Wang (University of Queensland, Australien) und Can Li (Chinese Academy of Sciences und Dalian Laboratory for Clean Energy, China) entwickelt wurde.
Erfolgsgeheimnis ist ein photochemisch-chemischer Kreislauf, dessen Reaktionen über ein so genanntes Redoxpaar gekoppelt sind. Ein Redoxpaar ist die Kombination einer reduzierten und einer oxidierten Form desselben Elements, die leicht ineinander umgewandelt werden können. Die Forscher setzten für ihren Ansatz entweder das Paar aus zweiwertigen und dreiwertigen Eisenionen (Fe2+/Fe3+) oder das System Iodid/Triiodid (I−/I3−) ein.
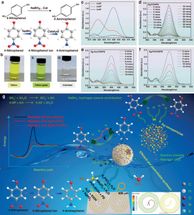
Das Schwefelwasserstoffgas wird in den Elektrolyten des Anodenraums einer elektrochemischen Zelle eingeleitet. Hier wird es durch eine chemische Reaktion mit der oxidierten Form des Redoxpaares, die dabei reduziert wird, gebunden und zu Schwefel, der als gelber Feststoff ausfällt, und Wasserstoffionen umgesetzt. Diese können die halbdurchlässige Membran zwischen Anoden- und Kathodenraum passieren. Die zweite Reaktion läuft photoelektrochemisch: Während Wasserstoffionen an der Kathode unter Aufnahmen von Elektronen zu Wasserstoff reduziert werden, wird die reduzierte Form des Redoxpaares durch Elektronenabgabe an die Anode wieder in den oxidierten Zustand gebracht. Treibende Kraft ist Sonnenlicht, das in der Photoanode Paare aus Elektronen und „Elektronenlöchern“ erzeugt, die dann durch die aufgenommenen Elektronen wieder aufgefüllt werden können.
Die Redoxpaare durchlaufen einen ständigen Kreislauf zwischen oxidierter und reduzierter Form, sodass als Gesamtreaktion die Spaltung von Schwefelwasserstoff in Schwefel und Wasserstoff durch Sonnenlicht resultiert.