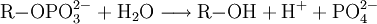Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Alkalische Phosphatase
Die Alkalische Phosphatase (AP, ALP, knochenspez. auch Ostase) ist ein Phosphorsäureester hydrolysierendes Enzym (Hydrolase). Die Alkalische Phosphatase entfernt Phosphat-Gruppen (Dephosphorylierung) von vielen Arten von Molekülen wie Proteinen, Nukleotiden und Alkaloiden. Sie arbeiten am effektivsten bei einem alkalischen pH-Wert. Produkt-Highlight
ReaktionDie alkalische Phosphatase hydrolysiert Phosphorsäureester zu Phosphat und Alkoholen, wobei Protonen entstehen. Dieses Enzym arbeitet nur in schwach alkalischer Lösung. Gäbe man das Enzym zu einer ungepufferten Lösung, so käme die Reaktion wegen der Protonenfreisetzung zum Stillstand. In vitro kann sie also nur in Gegenwart eines Puffers von geeigneten pH-Wert verfolgt werden. Das humane EnzymIm Menschen werden 15 verschiedene Isoenzyme unterschieden. Vier dieser Isoenzyme stammen von unterschiedlichen Genen (Dünndarm-AP, Plazenta-AP, Keimzell-AP und Gewebe-unspezifische AP). Die Gewebe-unspezifischen AP wird je nach Gewebe unterschiedlich glykosyliert, d. h. erhält unterschiedliche Zuckerketten. Dadurch entstehen weitere Isoenzyme (Leber-AP, Knochen-AP, Nieren-AP). LabordiagnostikDie Gesamtheit dieser Enzyme wird als „alkalische Phosphatase“ bei Standard-Blutuntersuchungen gemessen und kann Hinweise auf vorliegende Krankheiten der Leber und des Skeletts liefern. Referenzbereichfür Messungen bei 37 °C nach IFCC:
InterpretationAlkalische Phosphatasen sind in großer Menge im Skelettsystem, im Leberparenchym und in den Gallenwegsepithelien vorhanden. Demnach können zu hohe Werte ihre Ursache z. B. in Erkrankungen der Leber, der Galle, der Schilddrüse oder der Bauchspeicheldrüse haben. Auch bei Knochenerkrankungen wie Osteomalazie, Knochenmetastasen, Hyperparathyreoidismus oder auch bei Knochenbrüchen ist der Wert der AP in der Regel erhöht. Eine der häufigsten Ursachen für eine AP-Erhöhung sind maligne Tumoren, die in den Knochen metastasiert sind (Knochenmetastasen). Grundsätzlich weisen sowohl Kinder im Wachstum als auch Frauen im letzten Schwangerschaftsdrittel höhere aP-Werte auf; dies ist jedoch normal und liefert keinen grundsätzlichen Hinweis auf eine Erkrankung. Ein zu niedriger Gehalt an alkalischer Phosphatase findet sich z. B. bei der seltenen Erbkrankheit Hypophosphatasie; darüber hinaus als Begleiterscheinung eines Vitamin-C-Mangels (Skorbut), als Folge einer Bypass-Operation, bei Schilddrüsen-Unterfunktion (Hypothyreose), Morbus Wilson, schwerer Blutarmut, Magnesium-Mangel und bei Einnahme von Kontrazeptiva. Bei der CML finden sich erniedrigte alkalische Phosphatase-Werte in den Granulozyten. Anwendung in der BiologieIn der Biochemie wird die Alkalische Phosphatase in Verbindung mit einem chromogenen Substrat für verschiedene Nachweismethoden (Färbungen) eingesetzt:
Als chromogenes Substrat wird hierbei häufig BCIP in Verbindung mit NBT verwendet, welches von der Alkalische Phosphatase zu einem blauen Indigo-Farbstoff umgesetzt wird. In der Molekularbiologie wird die Alkalische Phosphatase aus Kälberdarm (Calf Intestine Alkaline Phosphatase) und aus Garnelen (Shrimp Alkaline Phosphatase) zur Dephosphorylierung von linearer DNA eingesetzt. Die gebräuchlichsten Alkalischen Phosphatasen sind:
Literatur
Siehe auch
|
|||||||||||||||
| Dieser Artikel basiert auf dem Artikel Alkalische_Phosphatase aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | |||||||||||||||